1. Introduktion til lægemiddeludvikling
Du har sikkert på et tidspunkt i dit liv brugt en form for lægemiddel – uanset om det har været en simpel hovedpinepille, antibiotika mod en bakteriel infektion, antihistamin mod allergi eller noget helt fjerde. Du kan sikkert komme i tanke om mange andre former for medicin, som du enten har brugt eller hørt om, og det burde være tydeligt, at lægemidler kan have mange forskellige funktioner.
En generel definition er: ”Et lægemiddel er et produkt, som er bestemt til at blive tilført mennesker eller dyr for at forebygge, lindre, behandle eller helbrede sygdom, sygdomssymptomer og smerter eller for at påvirke legemsfunktioner.” Selvom denne definition er letforståelig, er den bred nok til at tillade en stor gruppe af meget forskellige kemiske stoffer at blive anvendt som netop lægemidler.
Det kræver en interdisciplinær forståelse og kreativitet at udvikle nye lægemidler, og der vil undervejs i processen uden tvivl opstå problemer. Disse problemer kan være af forskellig art, og mange vil være betydelige nok til, at produktet aldrig bliver markedsført. Udfordringer i processen kan bl.a. omfatte:
- Komplikationer ved optagelsen af lægemidlet i kroppen
- Toksiske, altså giftige, bivirkninger
- Utilstrækkelig affinitet, dvs. at det aktive stof i lægemidlet ikke binder tilstrækkeligt til sit target
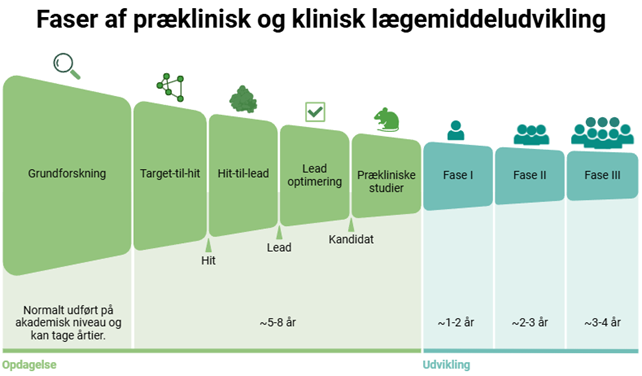
På grund af disse udfordringer er det under 1% af alle lægemidler, der bliver godkendt til markedsføring. Fremstillingen af lægemidler er en dyr proces, og fordi så få lægemidler når ud på markedet, betyder det, at det er en kostbar investering. I Figur 1 ses et estimeret antal lægemiddelkandidater på tværs af de overordnede dele af lægemiddeludvikling.

Overordnet proces og tidslinje
Når man skal udvikle et nyt lægemiddel, starter det hele med grundforskning. Dette er også idéfasen, hvor den første udgave af lægemidlet enten bliver udvundet (fundet i naturen) eller syntetiseret (i et laboratorie). Ofte er formålet at finde en løsning på, hvordan vi kan hjælpe kroppen med at bekæmpe en kendt sygdom eller bivirkninger, der forstyrrer vores dagligdag. Det er essentielt at udvælge det rigtige target, eftersom lægemidlet skal designes efter dette target.
Et target er det sted i kroppen, hvor et lægemiddel skal binde sig for at give den ønskede effekt. Et target kan være mange ting, men er stort set altid et eller flere proteiner i kroppen. Dette kan du læse mere om under den næste underside: “Proteiner som drug targets”.
Når vi har fundet et target, kan vi udvikle de første versioner af vores lægemiddel. Disse er ofte kendt som hits. Når vi arbejder videre i laboratoriet, kan hits videreudvikles til leads og til sidst til lægemiddelkandidater. Når man udvikler ny medicin i laboratoriet, starter man med in vitro-eksperimenter. Dette er en bred betegnelse for eksperimenter udført uden en levende organisme. Hvis en lægemiddelkandidat viser lovende resultater, er næste step in vivo-eksperimenter. In vivo er en betegnelse for eksperimenter udført på dyr. Valget af dyreart afhænger af, hvad man ønsker at undersøge. Dyrenes størrelse påvirker også omkostningerne ved forsøget samt kravene til de nødvendige tilladelser.
Efter det, der samlet set kaldes prækliniske studier, kan et lægemiddel testes yderligere via kliniske studier. Det er her, vi for første gang afprøver lægemidlet på mennesker. De kliniske studier opdeles overordnet i fire faser, hvoraf de første tre udføres inden godkendelse. Fase IV finder sted efter godkendelse og markedsføring, da medicinalvirksomheden er forpligtet til at overvåge langtidsbivirkninger.
- Fase I: 20-100 forsøgspersoner, alle frivillige, raske, unge mænd
- Fase II: 100-300 forsøgspersoner, en mindre gruppe syge patienter
- Fase III: 100-1000 forsøgspersoner, en stor og divers gruppe syge patienter
- Fase IV: 1000+ forsøgspersoner, almindelig brug efter godkendelse og markedsføring
Faserne i lægemiddeludviklingsprocessen op til godkendelse af lægemidlet er illustreret i Figur 2, hvor de vigtigste dele er inkluderet.
Hvorfor bruger man raske unge mænd i stedet for syge patienter i fase I?
I fase I testes et nyt lægemiddel primært for sikkerhed, ikke effektivitet. Raske unge mænd har en mere stabil fysiologi uden underliggende sygdomme, der kan påvirke resultaterne. Dette gør det lettere at identificere eventuelle bivirkninger og bestemme, hvordan kroppen optager, fordeler, metaboliserer og udskiller lægemidlet. Se mere om dette på undersiden “Lægemidlers vej gennem kroppen”. Desuden undgår man risikoen for, at eksisterende sygdomme eller anden medicin påvirker lægemidlets virkning.
Kan en farmaceutisk virksomhed frasige sig ansvar fra et lægemiddel, efter det er blevet godkendt til brug?
Nej, en farmaceutisk virksomhed kan ikke frasige sig ansvar for et lægemiddel efter det er godkendt. De har fortsat ansvar for sikkerhed, effektivitet og korrekt mærkning, og kan holdes ansvarlige, hvis der opstår problemer som ikke var kendte ved godkendelsen.
2. Proteiner som drug targets
For at udvikle et nyt lægemiddel er det nødvendigt at have viden om den sygdom, der skal behandles, samt det target, der skal rammes. Et target kan være mange forskellige biomolekyler, men i langt de fleste tilfælde er det et protein. Derfor er det vigtigt at have en grundig forståelse af proteiner og deres funktion for at kunne designe et specifikt lægemiddel, der kan interagere med target.
Der findes mange forskellige proteiner, hvoraf enzymer, receptorer og transportproteiner er særligt vigtige, da de udgør langt de fleste targets for de lægemidler, vi kender i dag. Udover proteiner findes der også andre typer drug targets, såsom DNA og RNA.
Uanset hvilket target der påvirkes, kan brugen af lægemidler føre til konsekvenser såsom udvikling af tolerance og afhængighed.
Enzymer
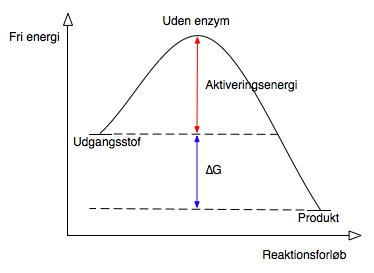
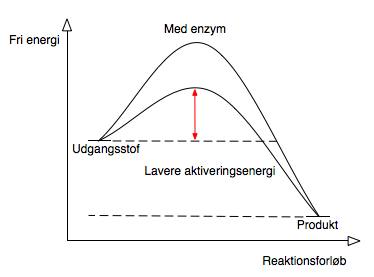
Et enzym er et protein, som fungere som en katalysator for biologiske processer. Enzymer kan ikke få reaktioner, der normalt ikke vil forløbe, til at ske, men de kan øge reaktionshastigheden i begge retninger for reaktioner, der vil normalt vil forløbe men virker ved at sænke aktiveringsenergien så en ligevægt indstille sig hurtigere, uden at påvirke hvor ligevægten er eller selv at blive forbrugt under processen, se figur 3.
Ligesom andre proteiner, består enzymer af af aminosyrer koblet sammen med peptidbindinger som er foldet i en bestemt tredimensionel struktur. Den tredimensionelle struktur er med til at skabe det aktive site, hvor et eller flere meget specifikke substrater passer ind, og kan bindes grundet de intermolekylære bindinger der kan ske mellem de substratet og aminosyrerne i det aktive site. Det er i det aktive site enzymet kan udføre sin funktion. Den tredimensionelle struktur kan også skabe hvad der er kendt som et allosteriske site, som kan ændre strukturen af det aktive site. Når et enzym benyttes som et drug target er vi derfor oftest interesserede i at finde et lægemiddel der kan fungere som substrat i det aktive site eller som kan bindes til det alleosteriske site.
- Reaktion mellem to molekyler i en opløsning: Enzymet opsamler de to rigtige molekyler og placere dem korrekt i forhold til hinanden, så de har nemmere reagere.
- Enzymet gør de kovalente bindinger i substratet svagere, da enzymerne trækker i bindingerne. Dette gør en deling af substratet i to lettere.
- Enzymer kan tilføre midlertidige funktionelle grupper til substratet. Dette sker vha. R-grupperne i enzymet, der kan ”overføre” deres funktionelle gruppe eller dele af dem til substratet. Herefter sker der en række reaktioner, således at enzymets funktionelle grupper bliver gendannet.
Induced fit
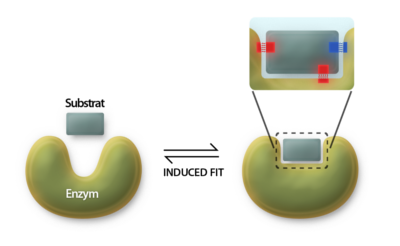
Når et substrat nærmer sig et tomt aktivt site på et enzym, interagerer det med enzymet og binder sig. Denne binding fremkalder en konformationsændring i enzymet, som er det, der beskrives som induced fit, se figur 4. Enzymet ændrer form, hvilket gør, at det bedre kan “lukke sig” omkring substratet. Denne ændring skaber de nødvendige bindinger for at katalysere reaktionen.
En vigtig del af denne proces er, at enzymets konformationsændring presser vand ud af det aktive site. Vand kan nemlig interferere med de bindinger, der skal dannes mellem enzymet og substratet (eller target-molekylet). Når vand er til stede, kan det danne hydrogenbindinger med target-molekylet og forhindre dannelsen af nødvendige bindinger til lægemidlet eller substratet.
Enzymkinetik
Enzymkinetik undersøger, hvordan enzymer reagerer på substrater og påvirkes af faktorer som substrat- og enzymkoncentration, samt hvordan inhibitorer kan hæmme enzymaktivitet. Når man snakker om lægemidler findes der overordnet set to typer:
- Agonister: Binder sig til en receptor eller et enzym og aktiverer det, hvilket fremkalder en biologisk respons, der efterligner den naturlige ligand.
- Antagonister: Binder sig til en receptor eller et enzym, men blokerer effekten af agonister eller naturlige molekyler ved at forhindre deres binding.
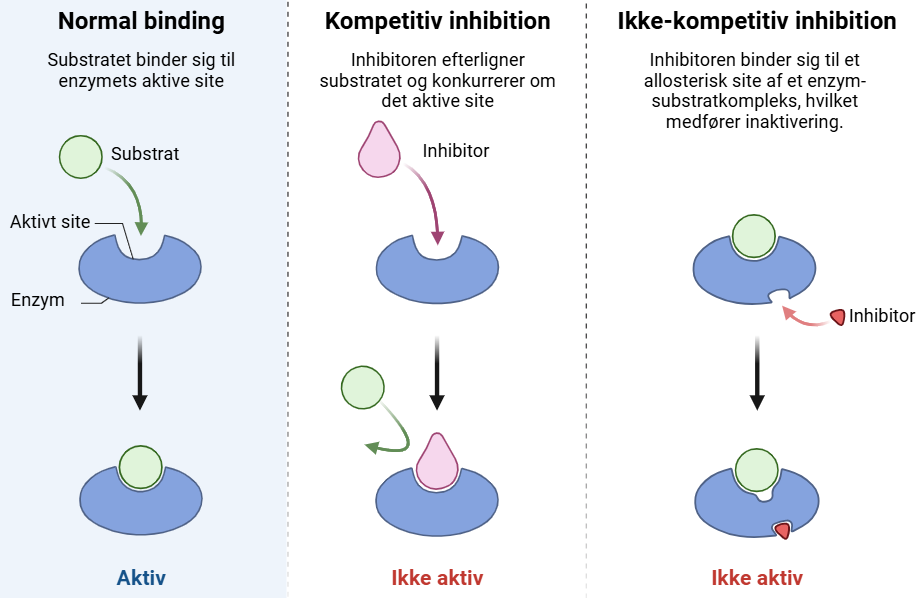
Inhibitorer fungerer som enzymernes antagonister. De binder sig til enzymets aktive site og hæmmer dets aktivitet, hvilket sænker reaktionshastigheden. Inhibitorer kan være irreversible (binder kovalent og hæmmer enzymet permanent, som nervegasser eller antabus) eller reversible (binder midlertidigt med ikke-kovalente bindinger), her henvises til illustration på figur 5.
Reversible inhibitorer: Binder midlertidigt til enzymet
- Kompetitiv inhibition: Inhibitoren konkurrerer med substratet om at binde til enzymets aktive site. Øget substratkoncentration kan overkomme hæmningen.
- Ikke-kompetitiv inhibition: Inhibitoren binder til det allosteriske site, hvilket ændrer enzymets tredimentionelle struktur og hæmmer dets aktivitet. Øget substratkoncentration kan ikke overkomme hæmningen.
Irreversible inhibitorer: Binder sig kovalent og permanent til enzymet og inaktiverer det, hvilket ikke kan overvindes ved at øge substratkoncentrationen.
Receptorer
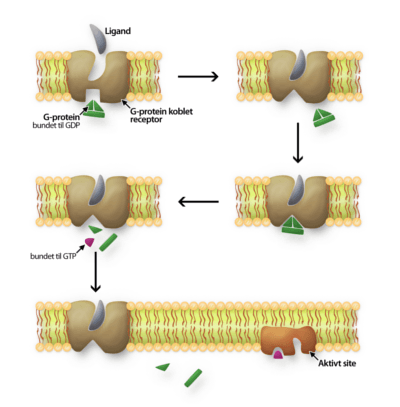
Receptorer ligner enzymer i deres opbygning, men er som regel placeret på cellemembranen. Ligesom enzymer indeholder receptorer også en kløft, hvor et molekyle kan binde sig. Kløften kaldes bindingssite, mens det i enzymer kaldes det aktive site. Grunden til, at det hos receptorer ikke kaldes et aktivt site, er, at der oftest ikke sker nogen omdannelse af et udgangsstof i dette område. Når en ligand (som svarer til et substrat for et enzym) binder sig til bindingssitet, sker der en konformationsændring, altså en induced fit. Dette sker hos alle receptorer, men hvad konformationsændringen medfører, kan variere.
G-protein koblede receptorer
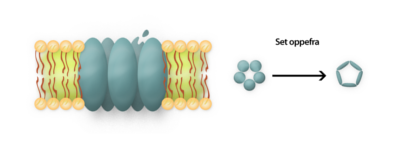
Ionkanaler
Transportproteiner
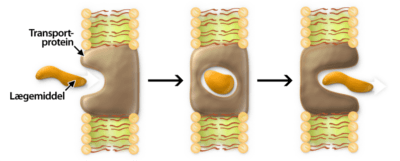
Transportproteiner er kroppens ”smuglere”, idet de smugler molekyler over cellemembraner, da molekylet i sig selv er for polært til at kunne krydse. Et transportprotein er derfor hydrofobt/upolært på ydersiden, så det kan sidde inde membranen, men er hydrofilt/polært på indersiden, så polære molekyler kan transporteres ind i proteinet. Transportproteinet lukker sig rundt omkring molekylet, der skal transporteres. Herefter bliver det transporteret igennem cellemembranen og sluppet fri på den anden side, se figur 8.
Et lægemiddel, der virker på et transportprotein, kan virke på forskellige måder. Lægemidlet kan virke ved selv at blive transporteret over cellemembranen ved at efterligne de molekyler, der normalt transporteres over membranen. Lægemidlet kan også virke ved at blokere transportproteinet og hæmmer derved optagelsen af det stof, som proteinet transporterer. Eksempelvis virker kokain i det centrale nervesystem ved at hæmme genoptagelsen af serotonin og dopamin gennem et transportprotein. Denne hæmning vil medføre, at der vil være mere serotonin og dopamin i synapsekløften mellem de to nerveender, og der vil derfor være et forlænget og øget signal gennem nerverne.
Tolerance og afhængighed
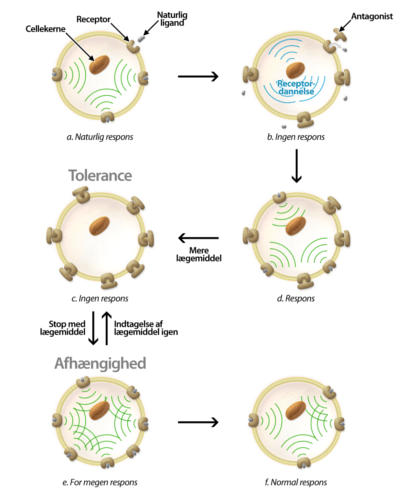
Hvis en celle udsættes for en antagonist i lang tid, vil cellen ikke modtage noget signal fra receptoren. For at kompensere for dette, vil cellen opregulere dannelsen af nye receptorer (figur 9b). Cellen kan nu igen registrere signaler fra den naturlige ligand (figur 9d). For at få den ønskede medicinske virkning vha. antagonisten, er man derfor nødt til at give en højere dosis af lægemidlet (figur 9c). Denne cyklus, hvor cellen danner flere receptorer, og der gives en højere dosis, kan blive ved med at gentage sig. Den tilstand cellen kommer i, og dermed også den tilstand kroppen kommer i, kaldes for tolerance, idet kroppen har brug for mere af lægemidlet for at opnå den ”normale” effekt.
Når indtagelsen af lægemidlet stopper, bliver alle receptorerne frigivet. Dette medfører, at alle de nye receptorer samt de oprindelige vil blive aktiveret af den naturlige ligand (figur 9e). Dette er meget ubehageligt, og man vil føle en trang til at tage stoffet igen, fordi det vil føles som et normalt respons. Dette kaldes for afhængighed, fordi man er nødt til at indtage lægemidlet for at have det godt. Over længere tid vil antallet af receptorer igen falde til et normalt niveau (figur 9f), men indtil da er patienten på afvænning.
3. Organisk kemi og lægemidler
For at udvikle effektive lægemidler er det afgørende at forstå det biologiske target, som lægemidlet skal interagere med. Targets er ofte proteiner, såsom enzymer eller receptorer, der spiller en central rolle i sygdomsmekanismer. Ved at kende de specifikke aminosyrer, der er involveret i bindingen mellem target og lægemiddel, kan denne viden anvendes til at designe lægemidler med høj specificitet og effektivitet.
En vigtig del af denne proces er valget af den rette grundstruktur og de rette funktionelle grupper i lægemidlets struktur. Disse grupper skal optimeres, så de kan danne de nødvendige kemiske interaktioner, såsom hydrogenbindinger, ionbindinger og hydrofobe interaktioner, med target. På denne måde kan lægemidlets affinitet og selektivitet forbedres, hvilket øger dets terapeutiske effekt og reducerer risikoen for bivirkninger.
Farmakofor og scaffold
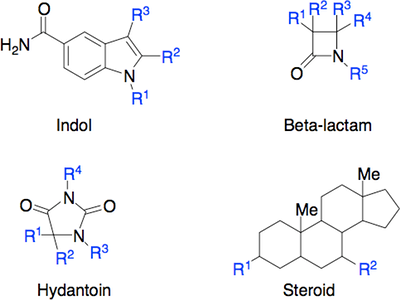
- Scaffold: Grundstruktur, som danner udgangspunkt for udvikling af et lægemidlet.
- Farmakofor: De funktionelle grupper i et lægemiddel, som er essentielle for dets aktivitet.
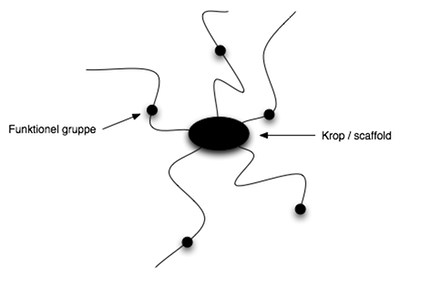
Farmakofor og scaffold kan illustres lidt ligesom en edderkop, se figur 10. Ved udvikling af et lægemiddel vælges først et scaffold – en lille grundstruktur med flere mulige bindingssteder for funktionelle grupper (R-grupper), se figur 11. Disse grupper sikrer optimal interaktion med target. Scaffoldet fungerer som en central enhed, hvorpå sidegrupper tilføjes baseret på deres evne til at danne intermolekylære bindinger med target. Disse bindinger adskiller sig fra de intramolekylære (kovalente) bindinger, der holder selve lægemidlets struktur sammen. De intermolekylære bindingstyper, som er afgørende for lægemidlets virkning, vil blive gennemgået herunder.
Hvorfor binder atomer sig overhovedet sammen?
Hvorfor vil atomer gerne ligne en ædelgas?
Hvorfor laver carbon fire bindinger?
Kan carbon danne dobbelt- eller trippelbindinger?
Hvordan påvirker valenselektroner antallet af bindinger?
Hvad kaldes de elektroner, der ikke indgår i bindinger?
Disse elektroner kaldes ledige elektronpar (eller lone pairs) og vises ofte som to prikker i forbindelse med atomet.
Bindinger
- Intramolekylære bindinger: Kovalente bindinger mellem atomerne i et molekyle
- Intermolekylære bindinger: Svagere bindinger mellem forskellige molekyler
Der findes fire forskellige intermolekylære bindinger, herunder Ionbindinger, Hydrogenbindinger, Dipol-dipol interaktioner og Van der Walls interaktioner, som alle binder til andre molekyler med forskellig styrke. De intermolekylære bindinger mellem et lægemiddel og dets target er særligt vigtige i lægeudviklingsprocessen. I tabel 1 kan der findes et overblik over de forskellige bindinger.
| Type | Styrke | |
| Intramolekylære | Kovalent binding | 200 – 450 kJ/mol |
| Intermolekylære | Ionbinding | 20 – 40 kJ/mol |
| Hydrogenbinding | 10-30 kJ/mol | |
| Dipol-dipol interaktion | 5-25 kJ/mol | |
| Van der Waals interaktion | 2-4 kJ/mol |
Tabel 1: Typer af intra- og intermolekylære bindinger, samt deres bindingsstyrke.
Polaritet
- Upolære bindinger: Når to atomer med næsten samme elektronegativitet binder sig sammen (differens <0,5), deler de elektronerne relativt ligeligt. Et eksempel på en sådan binding er mellem to hydrogenatomer (H-H), hvilket resulterer i en upolær kovalent binding. Molekyler som olie, der består af lange kæder af kulstof (C) og hydrogen (H), har generelt upolære bindinger.
- Polære bindinger: Hvis forskellen i elektronegativitet mellem to atomer er lidt større (0,5-2,0), vil elektronerne blive trukket lidt mere mod det mere elektronegative atom. Et godt eksempel på en polær kovalent binding er mellem oxygen og hydrogen i et vandmolekyle (H₂O). Den elektronegative forskel resulterer i, at oxygen trækker elektronerne mere mod sig, hvilket skaber en positiv ladning på hydrogenatomerne og en negativ ladning på oxygenatomet.
- Ionbindinger: Når forskellen i elektronegativitet er meget stor (>2), vil et af atomerne trække elektronerne helt til sig, hvilket resulterer i en ionbinding. Et eksempel er natriumchlorid (NaCl), hvor natrium (Na) afgiver en elektron til chlorine (Cl), og de danner ioner (Na⁺ og Cl⁻). I sådanne tilfælde er der ikke tale om en kovalent binding, men om en ionbinding, en væsentlig svagere binding, som vil brydes i en vandig opløsning.
Molekylers polaritet i relation til lægemidler:
Molekyler kan have både polære og upolære bindinger, og det er balancen mellem disse, der bestemmer, om et molekyle overordnet set er polært eller upolært. Molekyler, der primært består af kulstof og hydrogen, vil ofte være upolære, mens molekyler med mange oxygen- eller nitrogenatomer vil være mere polære. Desuden påvirker molekylets struktur også polariteten.
Når man designer et lægemiddel, er polariteten meget vigtig, især ved oral administration. Lægemidlet skal være polært nok til at kunne opløses i det vandige miljø i kroppen, men også upolært nok til at krydse cellemembraner og nå blodbanen. Hvis et molekyle er for polært, kan det have svært ved at passere cellemembranen, mens et for upolært molekyle kan have svært ved at opløses i vandige omgivelser, hvilket kan forhindre effektiv absorption i kroppen. Læs mere om cellemembraner og absorption af lægemidler under “Lægemidlets vej gennem kroppen”.
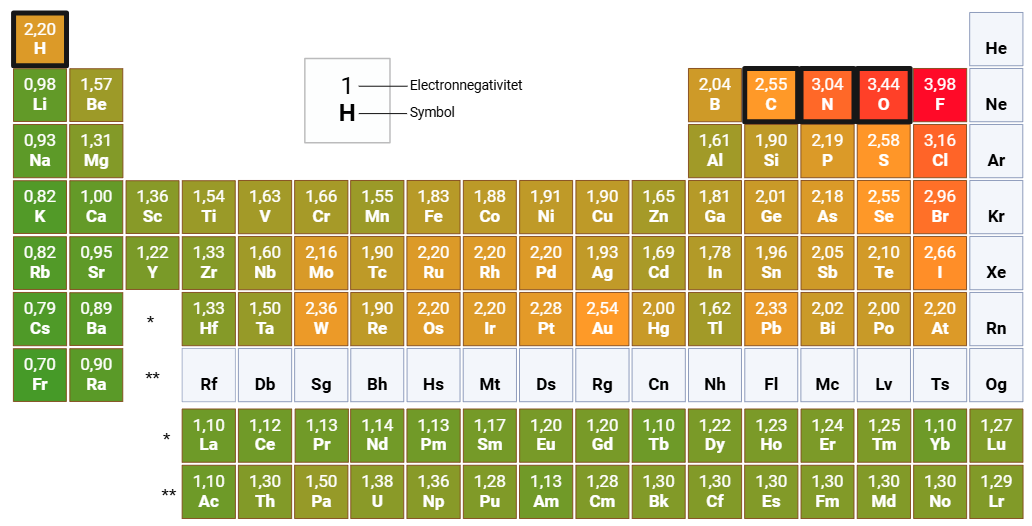
| Elektronegativitet | Polaritet |
| <0,5 | Upolær |
| 0,5 – 2,0 | Polær |
| >2,0 | Ionbinding |
Tabel 2: Sammenhæng mellem elektronegativitet og polaritet.
Intermolekylære bindinger
Ionbindinger
En ionbinding består af to modsat ladede ioner, fx Na⁺ og Cl⁻, som tiltrækkes af elektrostatisk kraft (figur 13). Ionbindinger er de stærkeste af de intermolekylære bindingstyper, men de bliver svagere, jo længere væk de ladede ioner kommer fra hinanden. Da ionbindinger er de stærkeste, er de ofte de første, der dannes, når et lægemiddel binder sig til sit target, hvilket kan hjælpe med at trække lægemidlet ind i den rette position.
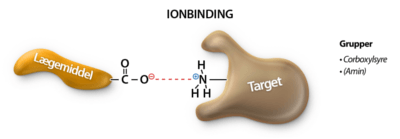
Van der Waals interaktion
Van der Waals-interaktioner, også kaldet London-bindinger, opstår i de hydrofobe dele af molekyler. Disse kræfter skyldes, at selv i molekylers neutrale og upolære områder vil der altid være en midlertidig ladningsforskydning på grund af de forskellige atomers elektronegativitet (figur 14). Dette skaber svage, midlertidige dipoler i molekylet. Når et lægemiddel og et target har modsatrettede ladningsforskydninger, kan de tiltrækkes af hinanden og danne en Van der Waals-interaktion. Selvom disse interaktioner er svage, spiller de en vigtig rolle i molekylers samspil og stabilisering.
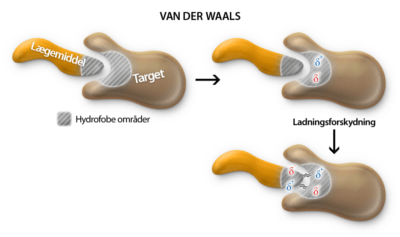
Hydrogenbindinger
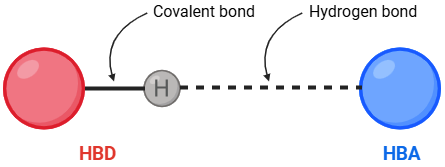
Hydrogenbindinger forekommer mellem to molekyler, hvor det ene molekyle har et elektronrigt atom, som oxygen eller nitrogen, der har et overskydende ledigt elektronpar og kan donere elektroner til et elektronfattigt hydrogenatom. Et elektronfattigt hydrogenatom er et hydrogenatom, bundet til et mere elektronegativt atom, som trækker elektronerne i bindingen mod sig selv, hvilket gør hydrogenatomet lettere positivt ladet. Denne positive ladning gør, at hydrogenatomet kan danne en binding med et elektronrigt atom i et andet molekyle (figur 15). Molekylet med det elektronfattige hydrogenatom kaldes en hydrogenbindingsdonor (HBD), da det donerer sit hydrogenatom, mens det elektronrige atom kaldes en hydrogenbindingsacceptor (HBA), da det accepterer et hydrogenatom. Funktionelle grupper som alkoholer (-OH) og aminer (-NH₂) fungerer som både donorer og acceptorer af hydrogenbindinger, da de indeholder både et elektronfattigt hydrogenatom og et elektronrigt atom som oxygen eller nitrogen.
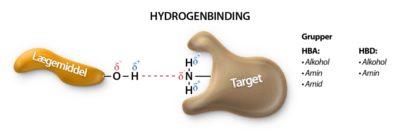
Dipol-dipol-interaktioner
Dipol-dipol-interaktioner opstår mellem molekyler, der har permanente dipoler, hvor der er en ulig fordeling af elektrisk ladning. Dette betyder, at molekylet har en positiv ende og en negativ ende, og disse poler tiltrækker hinanden. Den positive ende af et molekyle tiltrækker den negative ende af et andet molekyle, hvilket skaber en svag binding mellem dem.
I forhold til lægemidler kan dipol-dipol-interaktioner påvirke, hvordan et lægemiddel binder sig til dets target, da polære lægemidler kan danne disse interaktioner med polære dele af receptorer eller enzymer. Dette kan øge lægemidlets affinitet og selektivitet for dets target.
Isomeri
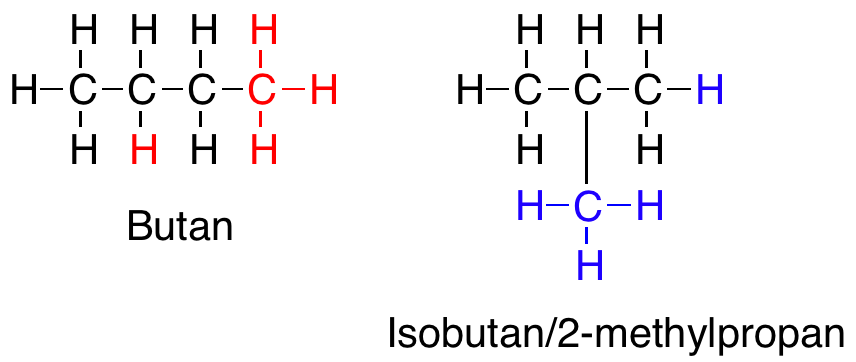
Isomeri beskriver forbindelser med samme kemiske formel, men forskellig opbygning, hvilket giver dem unikke fysiske og kemiske egenskaber. Organiske molekyler kan være forgrenede, som kan ses i figur 16, danne ringsystemer eller indeholde dobbeltbindinger, der kan resultere i cis-trans-isomeri.
Cis-trans-isomerer opstår, når to grupper sidder på samme side (cis) eller på hver sin side (trans) af en dobbeltbinding. Trans-isomerer har ofte højere smeltepunkter, da de er mere symmetriske og pakkes bedre i en krystalstruktur, mens cis-isomerer kan være mere polære.
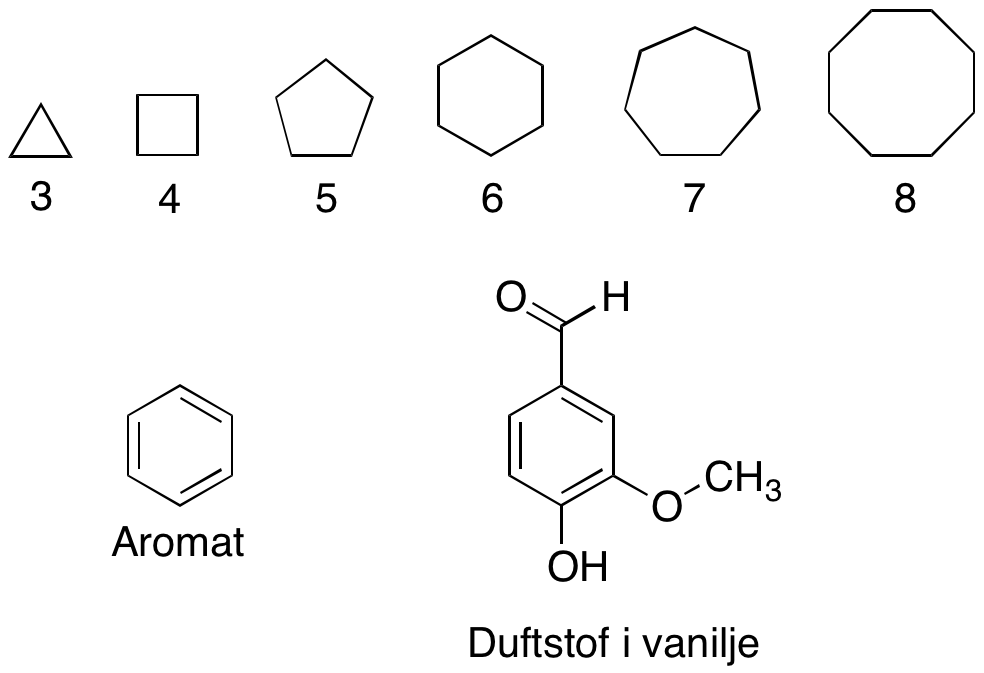
Ringsystemer findes i mange forskellige størrelser men typisk med fem eller seks carbonatomer, da disse er mest stabile. Aromatiske forbindelser består af en seks-leddet ring med tre konjugerede dobbeltbindinger. Navnet “aromat” stammer fra 1800-tallet, hvor disse forbindelser blev udvundet fra duftende planteekstrakter.
En aromatisk ring kan have forskellige sidegrupper bundet i bestemte positioner:
- Ortho (o-): Sidegruppen sidder direkte ved siden af en anden substituent.
- Meta (m-): Sidegruppen sidder to carbonatomer væk.
- Para (p-): Sidegruppen sidder tre carbonatomer væk eller lige overfor den anden substituent.
Se figur 17 for illustration af ortho-, meta- og para-substitution, samt andre ringsystemer.
Spejlbilledisomeri
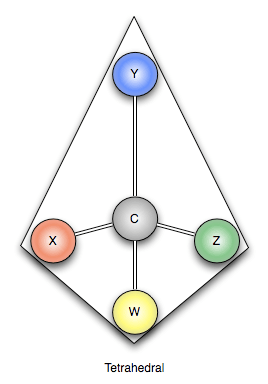
Stereokemi er den del af kemien, der beskæftiger sig med den tredimensionelle struktur af et molekyle. Der er flere former for stereokemi, fx cis-trans isomeri og spejlbilledisomeri. Her vil spejlbilledeisomeri kort blive beskrevet, da dette er yderst vigtigt for virkningen af lægemidler.
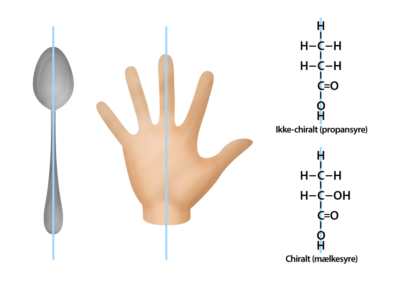
Hvis et carbonatom er bundet til fire forskellige atomer, kaldes det et stereocenter, og molekylet er ofte chiralt (se figur 18). Dette betyder, at et spejlbillede af molekylet ikke er identisk med det oprindelige, ligesom dine hænder ikke er ens. Molekylet er achiral, hvis der er et symmetriplan, der deler det i ens sider, som med en ske (se illustration i figur 19).
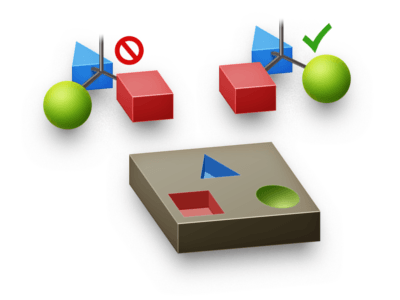
Enzymer og receptorer i kroppen er tilpasset de isomerer af deres substrater, der findes i naturen. For eksempel er alle aminosyrer (undtagen glycin) den samme isomer, og de enzymer, der nedbryder proteiner til aminosyrer, kan kun genkende denne form. Derfor er det vigtigt at tage højde for stereokemi i lægemiddeldesign. Hvis et lægemiddel ikke virker, kan det skyldes, at stereokemien ikke passer til targetets bindingssted, selvom den generelle struktur er korrekt (se figur 20)
Eksempel fra industrien: Citalopram
Det danske firma Lundbeck udviklede i 1989 et antidepressivt lægemiddel, som de kaldte for Citalopram. Citalopram har et enkelt stereocenter, som er angivet med en stjerne i figur 26, og citalopram er derfor et chiralt molekyle med to enantiomerer. Citalopram blev i første omgang markedsført som en blanding bestående af 50% af den ene enantiomer og 50% af den anden enantiomer, en racemisk blanding. Senere fandt Lundbeck ud af at det faktisk kun var den ene enantiomer der var ansvarlig for binding til target og dermed den biologiske virkning, nemlig (S)-(+)-citalopram. Lundbeck begyndte i stedet for at sælge denne ene enantiomer i den rene form, og kaldte nu i stedet lægemidlet for escitalopram. Resultatet af ændringen fra en racemisk blanding, hvor halvdelen af indholdet ikke var aktivt til et lægemiddel hvor alt indholdsstof er aktivt, er et lægemiddel der er langt mere potent og der derfor skal en lavere dosis til for at give den ønskede effekt. At have et mere potent stof er et vigtigt aspekt i lægemiddeludvikling, idet det er med til at mindske antallet og størrelsesordenen af uønskede bivirkninger.
4. Funktionelle grupper
Carbonhydrider
Carbonhydrider (Kulbrinter) er kemiske forbindelser, der kun består af carbon (C) og hydrogen (H). Disse forbindelser kan være alkaner, alkener, alkyner eller aromatiske forbindelser, afhængigt af typen af bindinger mellem kulstofatomerne. De forskellige carbonhydrider er illustreret i den grønne boks i figur 21. I denne figur kan det ses, at alkaner har enkeltbindinger, alkener har en dobbelbinding, og alkyner har en trippelbinding. Du kan huske navngivningen ved, at de er i alfabetisk rækkefølge (A, E, Y). En aromatisk ring er en ringstruktur, hvor kulstofatomer deler elektroner i et stabilt, delokaliseret elektronpar, hvilket giver særlig stabilitet. Et eksempel på en aromatisk ring er benzenringen, som består af seks kulstofatomer og seks hydrogenatomer.
Carbonyler
Carbonyler er funktionelle grupper, der indeholder et carbonatom, som er dobbeltbundet til et oxygenatom (C=O). Et udvalg af carbonyler er beskrevet herunder og illustreret i den orange boks i figur 21.
Ketoner
Carbonyler er funktionelle grupper, der indeholder et carbonatom, som er dobbeltbundet til et oxygenatom (C=O). Et udvalg af carbonyler er beskrevet herunder og illustreret i den orange boks i figur 21.
Aldehyder
Carboxylsyrer
Estere
Amider
Andre grupper
Alkohol
Ether
Halider
Halider er funktionelle grupper, der indeholder et halogenatom, såsom fluor (F), chlor (Cl), brom (Br) eller iod (I). En alkylhalid er en type halid, hvor et hydrogenatom i en alkan er erstattet med et halogen.
Brom- og iodholdige halider bruges sjældent i lægemidler, da de er meget kemisk reaktive. Halider reagerer med nukleofiler, hvorved nukleofilen bindes til molekylet, mens halogenet frigives. Halogenet optræder som elektrofil i denne reaktion, der betegnes som en substitutionsreaktion. Elektronerne fra nukleofilen bevæger sig over på halogenet, hvilket er karakteristisk for en SN2-reaktion. “S” står for substitution, “N” for nukleofil, og “2” angiver, at to molekyler afgør reaktionshastigheden (bimolekylær reaktion).
Amin
Aminer er funktionelle grupper, der indeholder et nitrogenatom bundet til en eller flere kulstofatomer. De kan fungere som hydrogenbindingsdonorer (HBD), hvis nitrogenatomet er bundet til et hydrogen, og som hydrogenbindingsacceptorer (HBA) via nitrogenatomets ledige elektronpar.
- Primære aminer: Nitrogen bundet til ét carbonatom og to hydrogenatomer.
- Sekundære aminer: Nitrogen bundet til to carbonatomer og ét hydrogenatom.
- Tertiære aminer: Nitrogen bundet til tre carbonatomer.
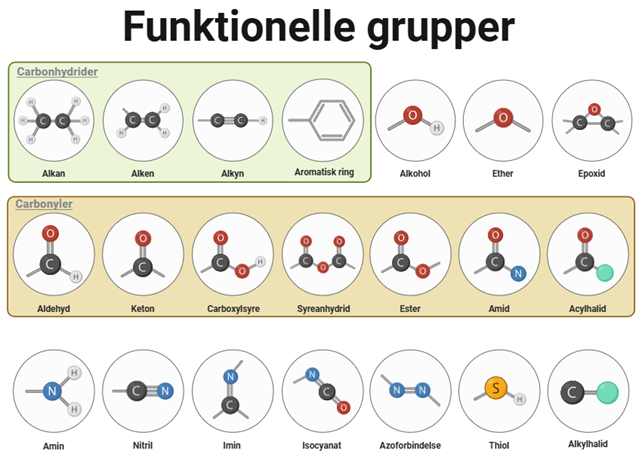
HBA og HBD
- Hydrogen Bond Acceptor (HBA): En gruppe eller et atom, der kan modtage en hydrogenbinding, typisk et oxygen- eller nitrogenatom med frie elektronpar. Market med blå på figur 21.
- Hydrogen Bond Donor (HBD): En gruppe eller et atom, der kan donere en hydrogenbinding, typisk en hydroxyl (-OH) eller amin (-NH) gruppe. Market med rød på figur 21.
Find alle HBA og HBD på figur 22
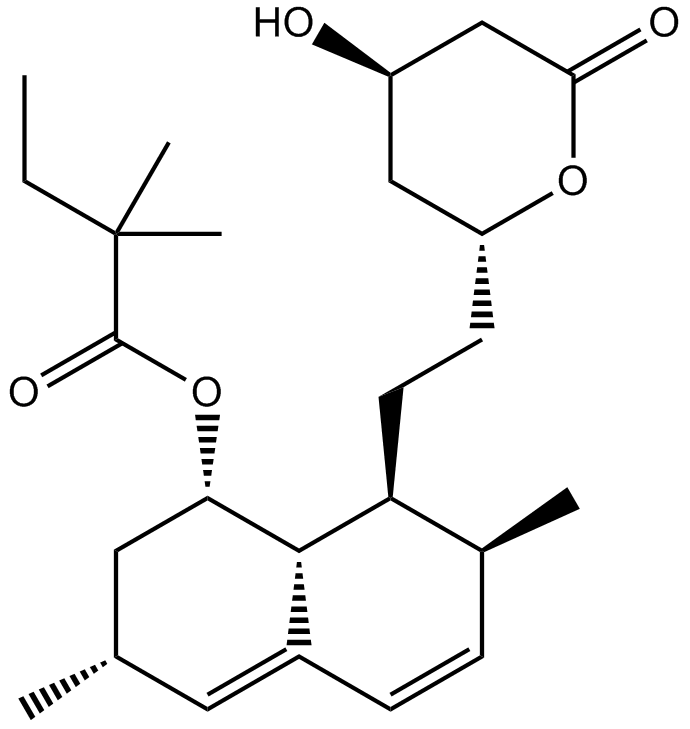
Vis svaret
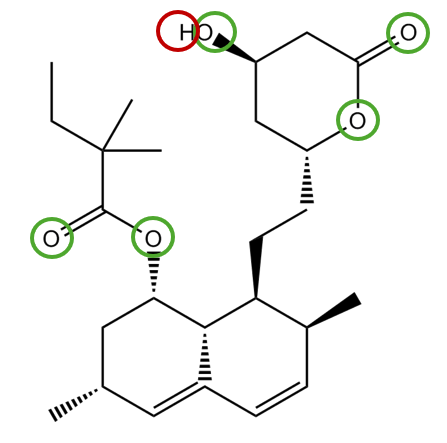
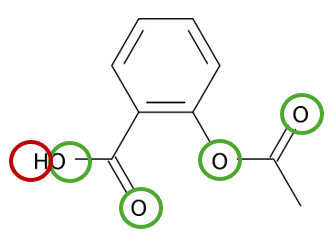
Find alle HBA og HBD på figur 23
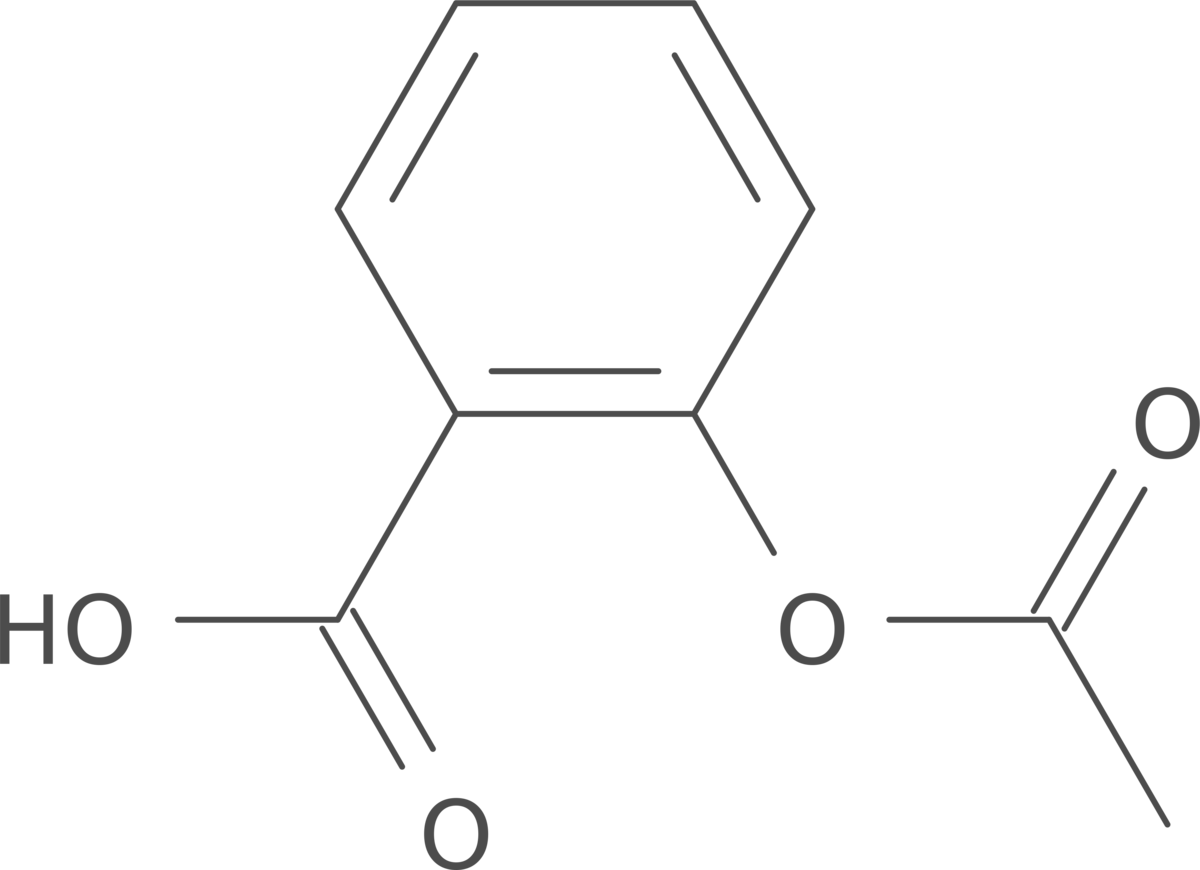
Vis svaret
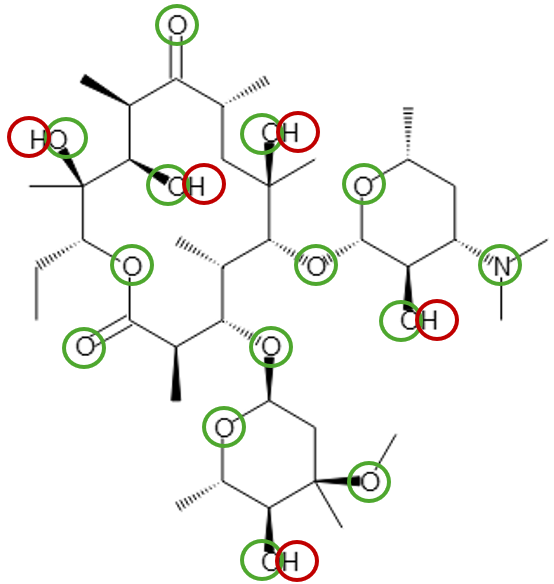
Find alle HBA og HBD på figur 24
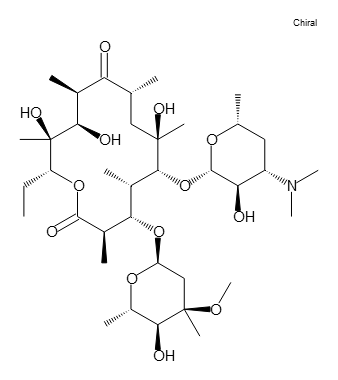
Vis svaret
5. Lægemidlers vej gennem kroppen
Inden et lægemiddel når frem til sit target, er der en række udfordringer på dets vej gennem kroppen, som det er vigtigt at tage højde for, når man designer lægemidlet. Disse udfordringer indebærer bl.a. mavesyren og fordøjelsesenzymerne, den cellemembran der skal krydses i tyndtarmen for at blive optaget i blodet, metaboliske enzymer i leveren samt at undgå at blive ophobet i fedtvæv. Det er vigtigt, at lægemidlet har en passende levetid, som sikrer, at dets optimale virkning. I den farmaceutiske industri benyttes begrebet farmakokinetik til at beskrive, hvordan kroppen påvirker et lægemiddel. Farmakokinetik beskriver absorption, distribution, metabolisme og ekskretion af et lægemiddel, hvilket betegnes som ADME. Et andet begreb er farmakodynamik, som beskriver, hvordan lægemidlet påvirker kroppen. Detaljer om både farmakokinetik og farmakodynamik kan findes i figur 25.
Anatomi
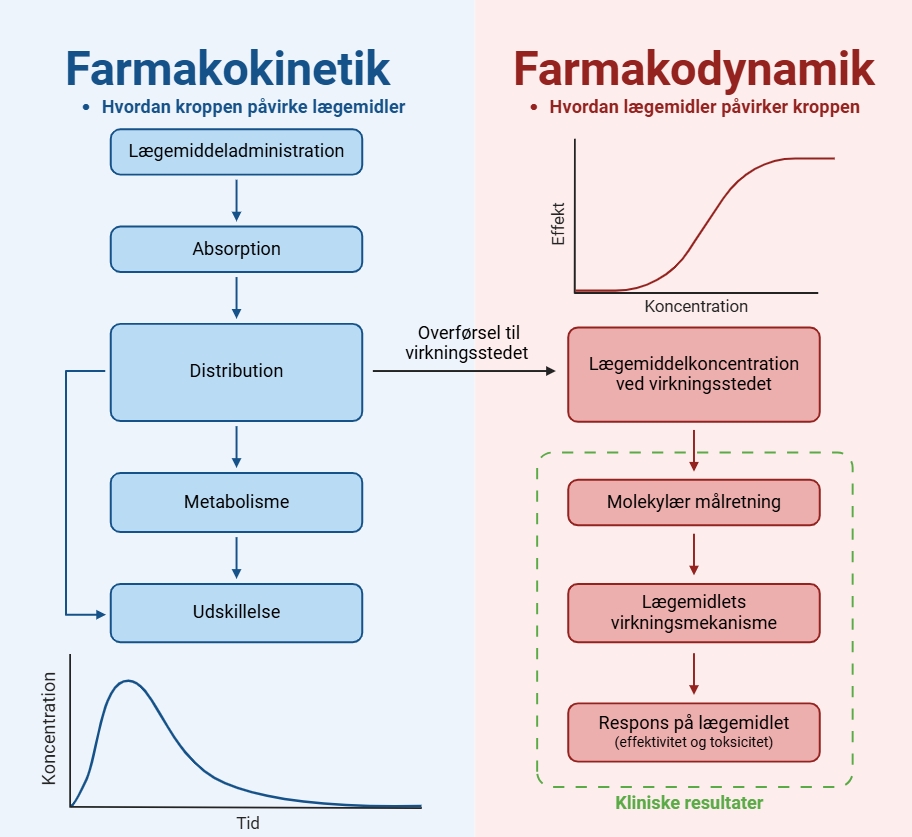
Når man designer et lægemiddel må man først og fremmest vide noget om, hvilke udfordringer et lægemiddel møder på sin vej gennem kroppen. Når et lægemiddel indtages oralt, kommer det igennem hele fordøjelseskanalen. Fordøjelseskanalen kan inddeles i mund, spiserør, mavesæk og tarm. Se også figur 26.
- I munden bliver lægemidlet udsat for de forskellige enzymer, der findes i vores spyt (primært amylase). Der er dog tale om ret små mængder af enzymer sammenlignet med den mængde af enzymer, som lægemidlet bliver udsat for senere.
- Herefter kommer lægemidlet videre til maven. I maven vil lægemidlet blive udsat for den meget surt miljø (pH = 1 – 3), der meget hurtigt kan nedbryde lægemidlet.
- Overlever lægemidlet dette, sendes det videre til tarmene, hvor det bliver udsat for en stor mængde fordøjelsesenzymer. Disse fordøjelsesenzymer nedbryder normalt den mad, vi indtager.
- Hvis lægemidlet har overlevet disse ”angreb”, er det nu tid til at krydse epitelcellelaget i tarmen for at trænge ind til blodbanen. For at kunne blive optaget i blodbanen, skal lægemidlet have den rette polaritet. Dette inkluderer, at lægemidlet skal være i stand til at kunne krydse cellemembraner, som er hydrofobe, men det skal også kunne befinde sig i blodet, som er hydrofilt.
Administration af lægemidler
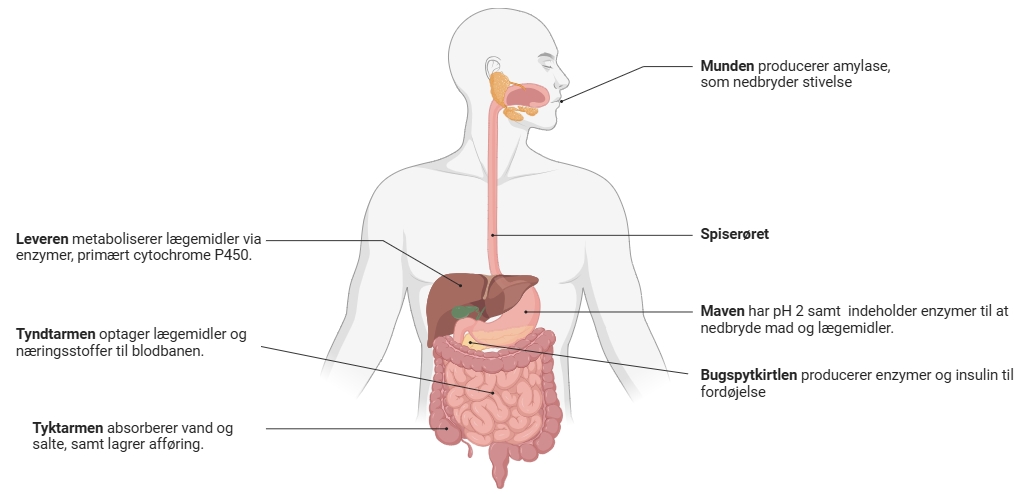
Et lægemiddel kan administreres på flere forskellige måder, heriblandt oralt, ved injektion, inhalation eller gennem huden (figur 27). Oral indtagelse af medicin i pilleform er langt den mest anvendte, idet det er den letteste, billigste og mest behagelige måde for patienten at tage medicin på. Men der er noget medicin, som ikke kan tages oralt. Dette kan skyldes flere ting, men ofte er det fordi medicinen enten bliver nedbrudt i fordøjelsessystemet eller ikke kan krydse epitelcellelaget i tarmen. Desuden er der en langt hurtigere virkning ved injektion, da medicinen kommer direkte ind i blodbanen, og der vil desuden være 100 % biotilgængelighed.
Administration af lægemidler kan også ske ved inhalation. Et kendt eksempel er ved astma, hvor lægemidlet skal virke lokalt i lungerne. Til sidst kan nævnes optagelse af lægemidler gennem huden. Dette kan være i form af nikotinplastre til rygestop, men også forskellige cremer, som fx. bedøvelsesmidler eller mod eksem, optages gennem huden. Optagelse gennem huden er en optagelseform, hvor stoffet skal diffundere over alle hudlagene, og virkningen af stoffet vil derfor indtræde langsomt samt vare i lang tid.
ADME
Absorption
Når et lægemiddel administreres oralt, skal det igennem en stor del af fordøjelsessystemet. Nogle lægemidler bliver optaget i mavesækken, men langt de fleste bliver optaget i tyndtarmen. Måden dette sker på, er, at lægemidlet skal bevæge sig hen over epitelcellelaget, altså krydse en cellemembran, og derved trænge ud i blodbanen, hvor det kan blive transporteret rundt i kroppen og nå dets target. Dette kaldes absorption af lægemidlet, og for at et lægemiddel kan tages oralt, er det nødvendigt, at det kan gennemgå dette trin.
Lipinskis regel af 5
Der er en række faktorer, der har indflydelse på, om et lægemiddel er i stand til at blive absorberet. Men overordnet set kan man benytte Lipinskis regel af 5 til at vurdere, om et lægemiddel kan absorberes, og dermed om det kan administreres oralt. Denne tommelfingerregel har fået sit navn, fordi alle punkterne går op i 5:
Molekylvægt (MW) <500 Da
Antal hydrogenbindingsacceptorer (HBA) < 10
Antal hydrogenbindingsdonorer (HBD) <5
Beregnet logP <5
Hvis et molekyle har logP >5, vil molekylet være for hydrofobt til at kunne opløses i vand. Molekylet vil derfor ikke kunne opløses i blodet, hvilket medfører, at det bliver tilbageholdt i cellemembranerne. Hvis logP derimod er meget lavt for et molekyle (<1), vil molekylet være for hydrofilt til at kunne krydse cellemembraner. Molekylet vil derfor ikke blive optaget i kroppen og vil blive udskilt uden at have udført sin virkning.
Syre/base kemi
Syre/base kemi er vigtig for forståelsen af, hvordan lægemidler absorberes i kroppen. Når et lægemiddel er ioniseret (ladet), kan det ikke passere cellemembraner, da kun uladede molekyler nemt kan diffundere igennem. Dette betyder, at syre/base-egenskaberne for et lægemiddel bestemmer, om det kan optages effektivt i tarmen. Syre/base-reaktioner og pH-værdien i kroppen afgør, om molekylerne er ioniserede eller uioniserede, hvilket påvirker lægemidlets absorption.
Hvad er syrer og baser?
Der findes flere forskellige definitioner af syrer og baser, fx Brønsted-Lowry- og Lewis-definitionerne. Brønsted-Lowry-definitionen er den mest anvendte og den generelle opfattelse af, hvad syrer og baser er. Ifølge Brønsted-Lowry er en syre et molekyle, der kan afgive en hydron (ioniseret hydrogen, H+), mens en base er et molekyle, der kan optage en hydron. Et molekyle kan også være både en syre og en base på samme tid. Vand er et eksempel, da det både kan afgive en hydron (og fungere som en syre):
$$H_2O rightarrow H^+ + OH^-$$
Reaktion 1. Vands reaktion som en syre.
Vand kan også optage en hydron og fungere som en base:
$$H_2O + H^+ rightarrow H_3O^+$$
Reaktion 2. Vands reaktion som en base.
Ligevægte
Når en kemisk reaktion forløber, vil der indstille sig en ligevægt. Dette gælder også for vands reaktion med sig selv. Når en ligevægt har indfundet sig, vil det sige, at reaktionen har nået et bestemt punkt, hvor der er lige meget omdannelse fra reaktant til produkt, som der er omdannelse fra produkt til reaktant. Reaktionshastigheden er derfor lige hurtig frem og tilbage, men der er ikke nødvendigvis lige meget produkt og reaktant.
Som beskrevet ovenfor består vand ikke kun af H2O-molekyler, men også af H+ og OH–. En ligevægt for H2O kan derfor skrives op på følgende måde:
$$H_2O rightleftarrows H^+ + OH^-$$
Reaktion 3. Ligevægt for H2O
Udregning af pH
pH er et mål for surheden i en opløsning og defineres som den negative logaritme af koncentrationen af hydroner (H₃O⁺):
$$pH = -log_{10}(H_3O^+)$$
Ligning 1. Formel for udregning af pH
Når vand blandes med en syre, opstår der en ligevægt, hvor vand enten afgiver eller optager hydroner. I tilfælde af en stærk syre vil ligevægten skubbe til højre, og al syren vil omdannes til sin konjugerende base. Hvis pH-værdien i en opløsning er kendt, kan man beregne koncentrationen af hydroner og dermed bestemme, hvor sur opløsningen er. En konjugeret base er den del af syren, der er tilbage, når syren afgiver en hydron (H⁺). På samme måde er den konjugerede syre den form, en base tager, når den optager en hydron.
pKs og pKb
Styrken af en syre kan beskrives ved syrestyrkekonstanten, Ks, som bestemmes ud fra ligevægten mellem syren og dens konjugerende base i opløsning. Syrestyrken angives ofte som pKs, hvilket er den negative logaritme til Ks:
$$pK_s = -log_{10}(K_s)$$
Ligning 2. Formel til beregning af pKS.
Stærke syrer har en lav pKs-værdi, mens svage syrer har en høj pKs-værdi. For baser kan styrken beskrives ved pKb, som bestemmes ud fra den korresponderende syres pKs-værdi ved følgende formel:
$$pK_b = 14 – pK_s$$
Ligning 3. Formel til beregning af pKb
Den konjugerede syre til en base er den form, basen optager, når den optager en hydron (H⁺). Omvendt er den konjugerede base den form, en syre tager, når den afgiver en hydron. Når pKs og pKb kendes, kan man forudsige, om et lægemiddel vil være ioniseret eller uioniseret i forskellige pH-områder i kroppen. Hvis pH-værdien i tarmen er passende i forhold til pKs, vil lægemidlet være uioniseret og kunne passere cellemembranerne. For svage baser vil det være muligt for dem at krydse tarmens celler, hvis pH er højere end pKb, mens svage syrer kræver en lavere pH for at forblive uioniserede og blive optaget i kroppen, disse kan derfor i nogle tilfælde blive optaget i mavesækken.
Partitionskoefficienten P (logP)
Nogle lægemidler er så hydrofobe, at de bliver fanget i cellemembraner og ophobes i fedtvæv. Andre lægemidler er så hydrofile, at de ikke kan krydse cellemembraner og derfor ikke kan optages oralt. En måde at vurdere, hvor hydrofobt eller hydrofilt et lægemiddel er (dvs. hvor opløseligt lægemidlet er i enten fedt eller vand), er ved at bestemme partitionskoefficienten P.
Partitionskoefficienten beregnes ved at placere molekylet i en blanding af 50 % octanol og 50 % vand. I et sådant system vil hydrofobe molekyler opholde sig i octanollaget, mens hydrofile molekyler vil befinde sig i vandlaget:
$$P = frac{text{Molekyle}_{text{octanol}}}{text{Molekyle}_{text{vand}}}$$
Ligning 4. Formel til beregning af partitionskoefficienten P. Firkantede parenteser bruges til at angive koncentrationer i de to faser, octanol og vand.
Som med de fleste andre fordelingskoefficienter angiver man ofte P som logP-værdien. Hydrofobe molekyler vil have en høj logP-værdi, mens hydrofile molekyler vil have en lav logP-værdi.
Man kan også bruge et computerprogram til at beregne en estimeret værdi, kaldet ClogP (calculated logP). Ligesom enkelte funktionelle grupper, såsom aminer, kan være både ioniserede og uioniserede, kan hele lægemidlet (inklusive dets funktionelle grupper) også være delvist ioniseret eller uioniseret. LogP-værdien angiver kun hydrofobiciteten af de uioniserede molekyler. Hvis man ønsker at måle de ioniserede molekyler, anvender man i stedet logD. I dette projekt benytter vi dog kun logP.
Distribution
Efter at et lægemiddel er optaget i blodet, skal det fordeles til de områder i kroppen, hvor det skal have sin virkning, det vil sige til de væv eller organer, hvor dets target er lokaliseret. Først passerer lægemidlet gennem leveren (se afsnittet om metabolisme), og derefter cirkulerer det i blodbanen. Fra blodet optages lægemidlet i de relevante celler i kroppen. Distributionen afhænger af lægemidlets kemiske struktur. Hvis lægemidlet binder sig stærkt til røde blodlegemer, kan det blive forhindret i at nå væv, hvilket kan være uønsket.
For at sikre, at et lægemiddel distribueres korrekt, er det vigtigt at balancere dets hydrofobicitet og hydrofilicitet. En for høj hydrofobicitet kan føre til, at lægemidlet ophober sig i fedtvæv, hvilket kan give uønskede bivirkninger. På den anden side, hvis et lægemiddel er for hydrofilt, kan det have svært ved at krydse cellemembraner. I sådanne tilfælde kan lægemidlet forblive i blodbanen i stedet for at blive distribueret til de steder, hvor det skal virke.
Metabolisme
Metabolisme foregår primært i leveren. Her findes en masse enzymer, som har til opgave at ændre strukturen af lægemidlet, så det kan blive udskilt fra kroppen. Lægemidler, der er meget polære, vil med det samme blive udskilt fra blodet gennem nyrerne og føres ud i urinen. Upolære molekyler er derimod vanskeligere for kroppen at udskille, men via metabolske processer, kan molekylet gøres mere polært, så det kan blive udskilt. Et metaboliseret molekyle kaldes for en metabolit. Når et lægemiddel bliver metaboliseret, vil det ofte miste sin oprindelige effekt. I nogle tilfælde kan metabolitten stadig have en smule aktivitet tilbage, men ændringen kan ogsåt føre til dannelsen af toksiske biprodukter, som kan forårsage uønskede bivirkninger. Det er derfor vigtigt at have kendskab til, hvilke metabolitter der kan dannes for at mindske toksiske bivirkninger. Der findes to primære former for metabolisme i leveren. Disse er kendt som fase I og fase II metabolisme, det er dog vigtigt at nævne at der foregår andre former for metabolisme forskellige steder i kroppen.
First pass effekt
Når et lægemiddel indtages oralt, transporteres det efter absorption gennem tarmbarairren, til den portale cirkulation, som leder blod fra tarmene til leveren. I leveren metaboliseres lægemidlet, hvilket resulterer i en lavere koncentration af det aktive stof i den systemiske cirkulation, som transporterer det videre til lægemidlets target. Ved intravenøs (i.v.) indsprøjtning går lægemidlet direkte i den systemiske cirkulation, hvilket betyder, at en større andel af det aktive stof, som når sit target, før det nedbrydes i leveren. Oralt administrerede lægemidler udsættes desuden for fordøjelsessystemets hårde miljø før absorption. Lægemidler administreret ved i.v. injektion vil have 100% Biotilgængelighed (andel af stoffet som når frem til systemisk cirkulation), mens både first pass effekt, miljøet i fordøjelsessystemet samt tarmbarairren medføre til at biotilgængeligheden for oralt administrerede lægemidler er væsentligt lavere.
Fase I
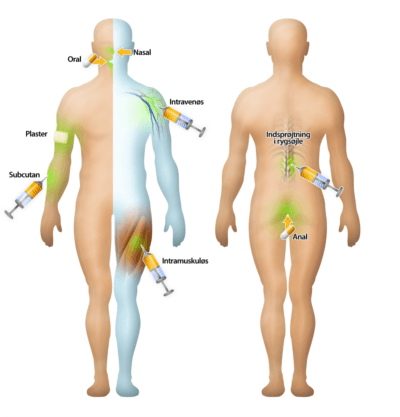
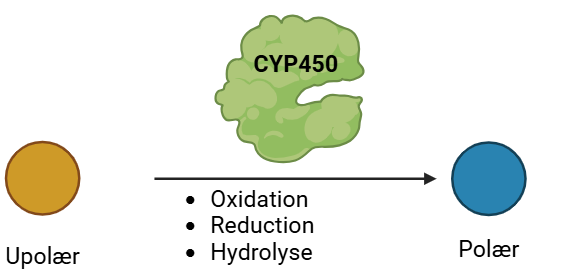
Fase I metabolisme omfatter primært oxidationsreaktioner, men kan også inkludere reduktion eller hydrolyse. Fælles for alle disse reaktioner er, at de katalyseres af cytochrom P450 (CYP) enzymer. CYP-enzymerne har til opgave at gøre molekylet mere polært, hvilket letter udskillelsen fra kroppen. CYP-enzymer er hæmproteiner, der indeholder en hæmgruppe og jern. De tilhører gruppen af monooxygenaser og benytter O2 fra leveren til at overføre et oxygenatom til lægemidlet, hvilket resulterer i oxidation. Det andet oxygenatom binder to hydrogenatomer og danner vand. For at oxidation kan finde sted, kræver CYP-enzymerne tilstedeværelsen af coenzymet NADPH, som bliver reduceret til NADP i processen. Fase I metabolisme er illustreret i figur 28.
Der findes mindst 33 forskellige CYP-enzymer, der hver varetager specifikke reaktioner. I de fleste fase I metaboliseringsreaktioner er det første trin tilføjelsen af en alkoholgruppe. Denne alkoholgruppe kan tilføjes på forskellige steder i et molekyle. Afhængigt af, hvor alkoholgruppen tilføjes, bliver OH-gruppen ofte oxideret til enten en keton eller en aldehyd. Hvis aldehyden dannes, vil den blive oxideret videre til en carboxylsyre. En funktionel gruppe, der kræver særlig opmærksomhed, er methylgrupper (CH3), da disse nemt oxideres til carboxylsyrer via sekundære alkoholer.
Fase II
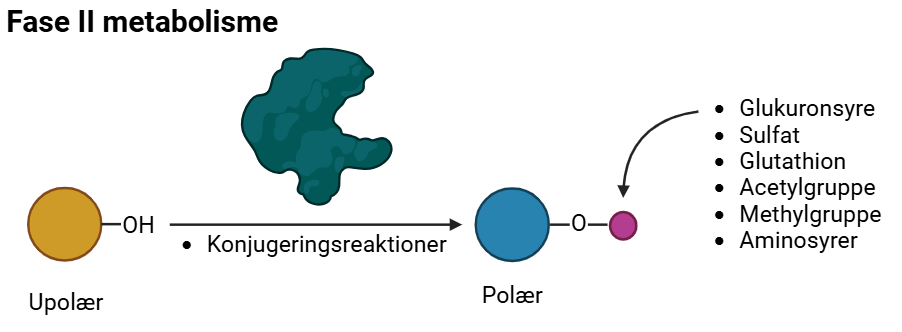
Fase II metabolisme består af konjugationsreaktioner, hvor en gruppe tilføjes molekylet for at øge dets polaritet, hvilket gør det lettere at udskille fra kroppen. Denne proces finder typisk sted efter fase I, men kan også ske uafhængigt.
Enzymerne, der er involveret i fase II metabolisme, tilhører transferase-enzymgruppen. Transferaser overfører grupper, som øger molekylets polaritet og gør det lettere at udskille via nyrerne eller galden. Eksempler på sådanne grupper inkluderer glukuronsyre, sulfatgrupper og methylgrupper. Et eksempel er dannelsen af O-glucuronider, hvor glukuronsyre tilføjes til et molekyle, ofte efter dannelsen af en hydroxylgruppe (OH) i fase I. Hvis lægemidlet indeholder en carboxylsyre, eller hvis en carboxylsyre dannes under fase I, kan en aminosyre, som ofte er glutamin, konjugeres til lægemidlet. På figur 29 er fase II metabolisme illustreret.
Andre former for metabolisme
Der findes også andre former for metabolisme, som ikke foregår i leveren. Forskellige oxidative enzymer, er fordelt rundt om i kroppens væv og deltager i fase I metabolisme af forskellige lægemidler. Desuden foregår der i blodet kemisk nedbrydning af funktionelle grupper uden enzymer. En af de mest markante kemiske nedbrydninger er omdannelsen af estre til carboxylsyrer og alkoholer. Denne mekanisme anvendes ofte i nedbrydningen af prodrugs til deres aktive form, se “Optimering af lægemidlet”.
Ekskretion
Ekskretion er processen, hvorved et lægemiddel fjernes fra kroppen. De fleste lægemidler udskilles via nyrerne gennem urinen, men op til 15% af et lægemiddel kan udskilles gennem sved. Nogle lægemidler kan også udskilles gennem lungerne, hvis de er i gasform, og den del af lægemidlet, der nedbrydes i fordøjelsessystemet, kan udskilles som afføring. I det følgende vil fokus være på udskillelse af lægemidler via nyrerne, da dette er den primære vej for lægemidler.
Hvorfor udskilles polære stoffer lettere end upolære stoffer i urinen?
6. Optimering af lægemidler
SAR
SAR (Structure-Activity Relationship) bruges i lægemiddeludvikling til at forstå, hvordan ændringer i et molekyles struktur påvirker dets biologiske aktivitet. Det handler om at identificere, hvilke funktionelle grupper der er nødvendige for at danne vigtige bindinger med target.
Eksempler på funktionelle grupper, der kan spiller en rolle i forbindelse med binding til target, inkluderer:
- Hydrogenbindende grupper: f.eks. -OH, -NH2, -COOH, som indeholder HBA og HBD er vigtige for at danne hydrogenbindinger.
- Ionbindinger: f.eks. Carboxylsyre (COOH) kan danne ionbindinger, som er vigtige for aktivitet.
- Van der Waals-interaktioner: Svage interaktioner mellem atomer i molekylet stabiliserer bindingen.
- Pi-stabling: Aromatiske grupper kan interagere med andre aromatiske grupper i target.
Et SAR-studie analyserer, hvordan ændringer i grupper som alkohol (OH), aminer (NH2), carboxylsyrer (COOH) og aromatiske ringe påvirker lægemidlets evne til at binde sig til target og fremkalde den ønskede effekt. For eksempel, hvis en alkoholgruppe fjernes og aktiviteten reduceres, betyder det, at gruppen er vigtig for bindingen. Hvis en aromatisk ring udskiftes med en cyclohexan-ring, og aktiviteten falder, kan det indikere, at Van der Waals-interaktionerne fra den aromatiske ring er nødvendige for effektiv binding. Figur 30 illustrerer disse et lægemiddel og de grupper der kan være vigtige for bindingen, samt analoger, hvor disse grupper er fjernet eller erstattet.
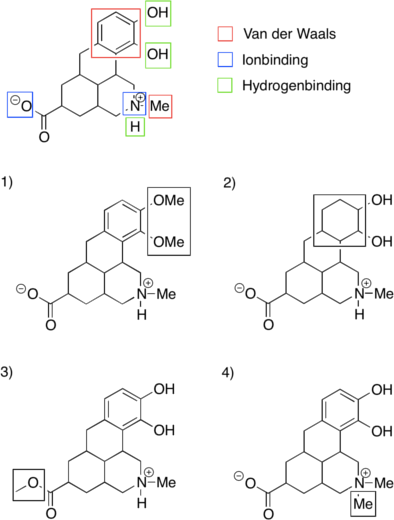
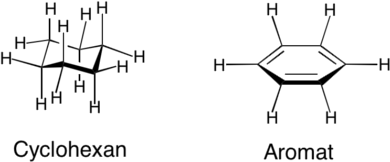
Hvorfor er der forskel i de intramolekylære bindinger, når en aromatisk ring udskiftes med en cyclohexanring?
Forskellen opstår, fordi den aromatiske ring kan danne stærkere hydrofobe interaktioner, pi-stabling og Van der Waals-interaktioner. Aromatiske ringe har en flad struktur, der muliggør stabile bindinger. Når den udskiftes med en cyclohexanring, fjernes de flade interaktioner og reduceres Van der Waals-kontakter, hvilket svækker bindingen og kan mindske aktiviteten.
Optimeringsstrategier
Target Binding: Rokering, Forlængelse og Udvidelse
Hvis et lægemiddel ikke har de rette interaktioner med sit target, selvom det indeholder de korrekte funktionelle grupper, kan strukturen optimeres. Optimeringen kan foretages på forskellige måder afhængigt af bindingens problem:
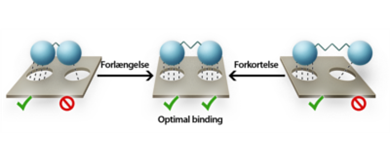
- Forskydning af funktionel gruppe: Hvis en funktionel gruppe på lægemidlet er forskudt i forhold til en gruppe i targetmolekylet, kan længden af carbonkæden justeres for at placere den funktionelle gruppe korrekt. (figur 31)
- Placering af funktionel gruppe: Hvis en funktionel gruppe er placeret et sted i molekylet, der forhindrer den ønskede interaktion med target, kan dens placering ændres for at sikre en bedre pasform. (figur 32)
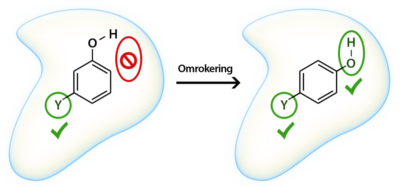
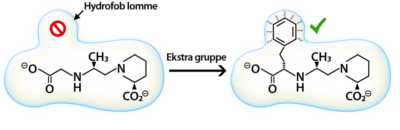
- Indsættelse af hydrofob gruppe: En ekstra hydrofob gruppe kan indsættes for at fylde en hydrofob lomme i targetmolekylet, hvilket kan forbedre bindingen. (figur 33)
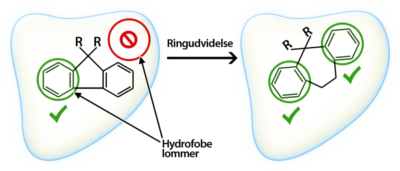
- Ringudvidelse: Hvis en del af molekylet ikke binder sig præcist til target, kan ringstrukturer udvides for at forbedre pasformen og bindingen. (figur 34)
Ændring af funktionelle grupper
En måde at forbedre et lægemiddel på er ved at ændre de funktionelle grupper, som molekylet allerede har. Hvis et lægemiddel har en funktionel gruppe, der gør det muligt at danne ionbindinger, men ikke hydrogenbindinger, kan man ændre gruppen til f.eks. en HBD (hydrogenbinding donor), så molekylet bliver i stand til at danne hydrogenbindinger med sit target. Dette kan være relevant, hvis lægemidlet skal binde sig til et target, der har en HBA (hydrogenbinding acceptor).
Bioisosterer
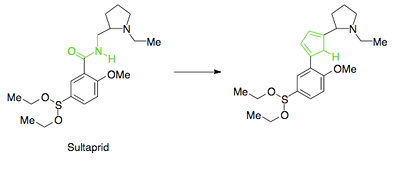
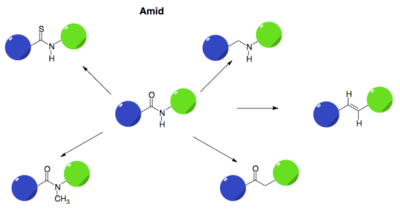
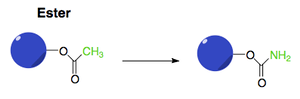
Bioisosterer er funktionelle grupper, der kan erstatte andre funktionelle grupper, men stadig bevare lægemidlets biologiske aktivitet og tredimensionelle struktur. Det betyder, at man kan ændre et molekyle uden at ændre på, hvordan det virker i kroppen. Et eksempel på dette er sultoprid, som er en dopamin-antagonist, se figur 35. I sultoprid er der en amidgruppe, der ligner en peptidbinding, som hurtigt bliver nedbrudt i kroppen. For at gøre lægemidlet mere stabilt kan man erstatte amidet med en pyrrolring, som har en lignende struktur. På den måde bevares lægemidlets funktion, men det nedbrydes langsommere i kroppen. I figur 36 er der vist forskellige eksempler på bioisosterer for amider.
Absorption/oplsøselighed
For at optimere et lægemiddel er det afgørende at justere molekylets polaritet og opløselighed, da disse faktorer påvirker dets absorption i kroppen.
Et molekyle, der er for polært (hydrofilt), vil nemt kunne opløses i kroppens vandige miljø, men vil hurtigt blive udskilt via nyrerne. For at undgå dette kan man skjule polære grupper, f.eks. ved at omdanne en alkohol til en ester eller ether, hvilket gør molekylet mindre vandopløseligt og dermed lettere at optage gennem cellemembraner. Omvendt kan et for upolært molekyle have svært ved at blive opløst i vandige miljøer og potentielt sidde fast i cellemembraner. En løsning kan være at tilføje polære grupper, men dette kan medføre uønskede interaktioner forskellige steder i kroppen. I stedet kan man modificere eksisterende grupper, såsom at ændre methylether til alkohol eller fjerne hydrofobe dele.
Det er desuden vigtigt at huske:
- Jævn fordeling af hydrofobe grupper: At have de hydrofobe grupper fordelt jævnt på molekylet sikrer effektiv optagelse gennem cellemembraner. Hvis disse grupper er ulige fordelt, risikerer man, at molekylet bliver fanget i membranen og derfor aldrig når sit target.
- pKa-værdien bør være mellem 6 og 9: Samlet set handler det om at finjustere molekylets struktur for at sikre, at det kan absorberes effektivt og nå sin målstruktur i kroppen.
Craig plot
Det kan være svært at vide, hvilke funktionelle grupper der skal ændres, eller hvad grupperne skal ændres til, for at øge aktiviteten af et lægemiddel. Et lægemiddel har nogle fysisk-kemiske egenskaber, som kan relateres til den biologiske aktivitet. Der er to fysisk-kemiske egenskaber, der er specielt vigtige i forhold til biologisk aktivitet:
Hydrofobiciteten af molekylets funktionelle grupper (π).
π > 0 angiver, at molekylet er hydrofobt.
π < 0 angiver, at molekylet er hydrofilt.
Hvor elektrondonerende eller -tiltrækkende en aromatisk substitut er i lægemidlet (σ)
σ > 0 betyder, at den aromatiske substitut er elektrontiltrækkende.
σ < 0 betyder, at den aromatiske substitut er elektrondonerende.
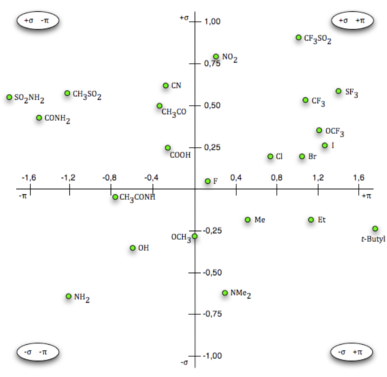
π og σ kan indtegnes i et diagram for forskellige funktionelle grupper, kaldt et craig plot. Ud fra et craig plot kan man danne sig et overblik over, hvilke funktionelle grupper man kan ændre de nuværende substituenter i et molekyle til, for fx at ændre hydrofobiciteten af molekylet. Figur 38 viser et craig plot for aromatiske substituenter i para-stillingen.
Eksempel: Hvordan du bruger Craig-plottet
Start med et lægemiddel med en t-butylgruppe. Denne gruppe gør molekylet meget hydrofobt og svært at optage i kroppen (høj logP-værdi, se Lipinskis regel af 5).
- Tjek Craig-plottet: T-butylgruppen ligger i 4. kvadrant og indikerer høj hydrofobicitet.
- Find en mindre hydrofob gruppe: Methylgruppen (Me) er mindre hydrofob end t-butylgruppen.
- Erstat t-butyl med methyl: Skift t-butylgruppen ud med methyl for at gøre molekylet mindre hydrofobt.
Molekylet bliver lettere at opløse i vand og lettere at optage i kroppen.
Topliss skema
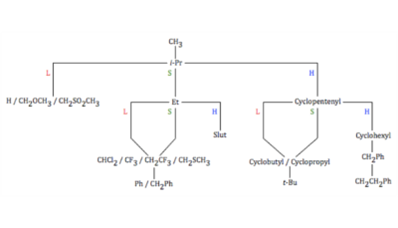
Udover at bruge et Craig-plot kan et Topliss-skema være nyttigt. Skemaet viser den næste analog, der skal testes for aktivitet, baseret på substitutternes π- og σ-værdier. For hver analog er der tre mulige udfald: højere, lavere eller samme aktivitet som det oprindelige molekyle. Den næste analog vælges ud fra aktivitetens grad. Der findes to Topliss-skemaer: ét for aromatiske substituenter (figur 39) og ét for carbon-sidekæder (figur 40).

Metabolisme
Visse funktionelle grupper, som estre, amider og methylgrupper, er særligt udsatte for metabolisme i kroppen. Dette fører til hurtig udskillelse via nyrerne og en kort halveringstid. En metode til at beskytte disse grupper mod metabolisme er ved at indføre sterisk hindring, hvor en kemisk gruppe placeres tæt på den udsatte funktionelle gruppe, så metaboliseringsenzymer ikke kan nå den. Alternativt kan de udsatte grupper fjernes eller erstattes med bioisosterer.
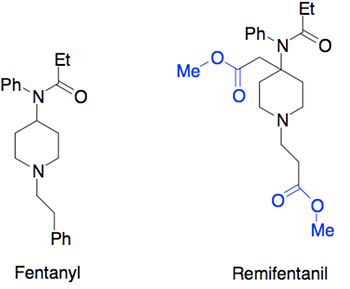
I visse tilfælde kan et lægemiddel have en for lang halveringstid i kroppen. Dette er gældende for fentanyl, et bedøvelsesmiddel brugt under operationer. Ved at fjerne en aromatisk ringe og indesætte to estre, fås lægemidlet remifentanil, se figur 41. Denne ændring betyder, at stoffet nedbrydes hurtigt i blodet og dermed giver en kortere virkning, hvilket er nyttigt til kortvarige operationer.
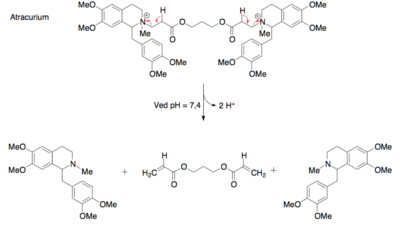
Et andet eksempel er atracurium, som er et “self-destruct” lægemiddel, se figur 42. Det er stabilt i mavesyren, men nedbrydes i blodet, hvor pH er mere neutral eller basisk, hvilket stopper dets virkning. Dette gør det velegnet til intravenøs administration, hvor doseringen kan justeres, og patienten kan vågne op hurtigt efter operationen.
Prodrugs
Prodrugs er lægemidler, der ikke har deres aktive kemiske struktur, når de indtages. Strukturen for disse lægemidler vil dog blive ændret på deres vej gennem kroppen, før de når target. Specielt i leveren vil stoffet blive udsat for metabolisk modificering. Efter denne proces recirkulerer stoffet i kroppen, såfremt det ikke udskilles, og da lægemidlet nu har fået sin aktive form, vil det udøve sin tilsigtede virkning.
Hvorfor anvendes prodrugs?
Prodrugs udvikles for at forbedre lægemidlers optagelse, fordeling, metabolisme og udskillelse (ADME):
- Nogle aktive stoffer har dårlig opløselighed eller optagelse i tarmen. Et prodrug kan designes til bedre optagelse.
- Ved at aktivere stoffet først på det ønskede sted i kroppen kan bivirkninger reduceres.
- Langsommere frigivelse af det aktive stof kan give en længere virkning.
Design af prodrugs
I designet af et prodrug er det vigtigt at tage højde for, hvilke metaboliseringer der finder sted i kroppen. En af de funktionelle grupper, som let bliver metaboliseret, er estre. Et lægemiddel, der indeholder en carboxylsyre, bliver ikke særlig godt optaget over tarmen. En metode til at forbedre optagelsen er at konvertere carboxylsyren til en ester, før lægemidlet indtages. Esteren hydrolyseres hurtigt tilbage til en carboxylsyre eller en alkohol, når lægemidlet kommer ind i blodbanen og leveren.
Eksempler på prodrugs
Acetylsalicylsyre (Aspirin®)
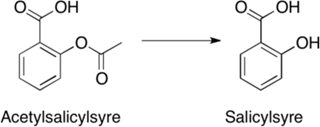
Salicylsyre er et smertestillende lægemiddel, men kan give blødninger i maven pga. dets fenolgruppe. Ved at omdanne det til en ester (acetylsalicylsyre) undgås dette problem (figur 43). Acetylsalicylsyre er ikke smertestillende i sig selv, men hydrolyseres i blodbanen til salicylsyre, der har den ønskede virkning.
Valaciclovir
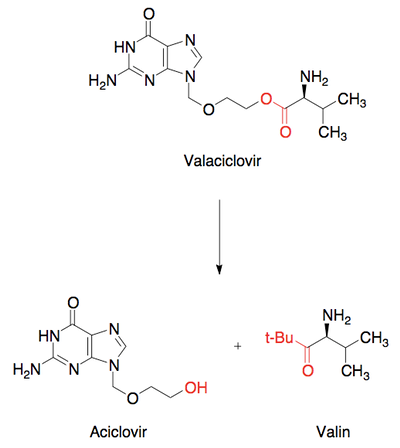
Bruges mod herpesvirus og omdannes efter optagelse til aciclovir. Aciclovir optages dårligt over tarmen, men valaciclovir har bedre optagelse og omdannes derefter til den aktive form (figur 44).
7. Eksempel 1 - En kur mod psoriasis
Psoriasis er en hudsygdom, hvor hudceller deler sig hurtigere end normalt, hvilket fører til tykke, skællende plamager. Dette afsnit omhandler hvordan lægemidlet Calcipotriol blev udviklet til behandling af psoriasis.
Opdagelsen af en potentiel kræftbehandling
I 1980’erne fandt forskere ud af, at vitamin D kunne hæmme væksten af visse kræftceller. Dette skabte håb om en mulig behandling, men der opstod et problem: Vitamin D regulerer også calcium i blodet. Når stoffet administreres i den relativt store mængde, der er nødvendig for effektiv behandling kan det føre til farlige bivirkninger, som følge af calcemisk effekt. Calcemisk effekt er når concentrationen af calcium i blodet stiger så meget at calcium udfælder og ophobede sig i kroppens organer.
For at løse dette problem begyndte forskere at udvikle en modificeret version af vitamin D, der kunne bevare den gavnlige effekt på cellevæksten uden at forårsage for meget calciumophobning. Dette skete gennem et såkaldt SAR-studie (Structure-Activity Relationship), hvor forskellige dele af vitamin D-molekylet blev ændret og testet.
Udviklingen af Calcipotriol
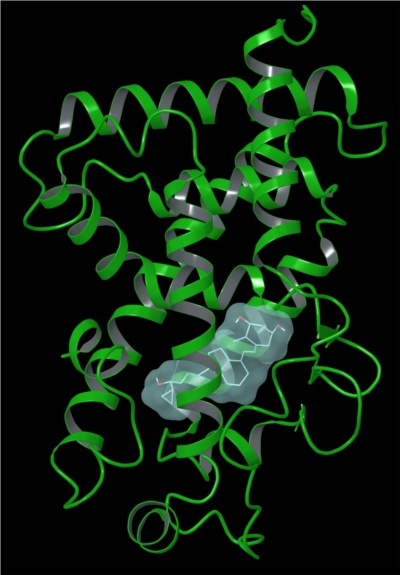
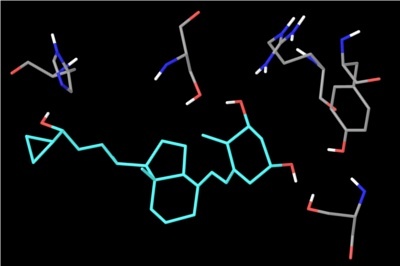
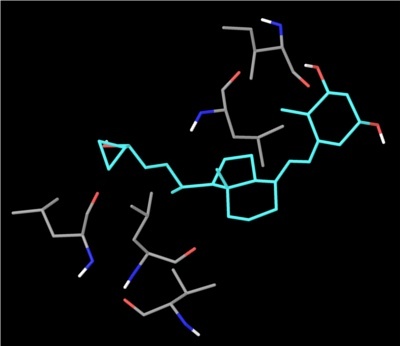
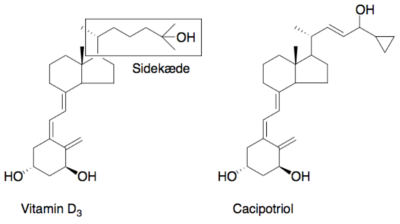
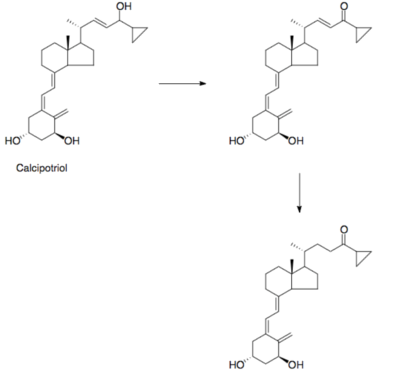
Efter mange forsøg lykkedes det forskerne at finde en vitamin D-analog, calcipotriol, der kunne hæmme cellevæksten uden at give farlige calciumrelaterede bivirkninger, se figur 45, hvor calcipotriol er bundet til vitamin D-receptoren. Se strukturene for vitamin D og calcipotriol på figur 46. Når calcipotriol binder til vitamin D-receptoren, bliver der dannet hydrogenbindinger som kan ses i figur 47, og nogle hydrofobe interaktioner som kan ses i figur 48. Desværre viste det sig, at calcipotriol blev nedbrudt for hurtigt i kroppen til at have en effekt som oral behandling mod kræft, og stoffet blev derfor droppet til dette formål.
Kort tid efter opdagede man dog noget interessant: En japansk patient, der fik vitamin D mod knogleskørhed, oplevede en markant forbedring af sin psoriasis. Samtidig fandt forskere ud af, at vitamin D-receptorer findes i hudceller. Dette fik forskere hos LEO Pharma til at undersøge, om calcipotriol kunne anvendes som en topisk behandling (creme) mod psoriasis.
Fra laboratoriet til godkendelse
Forskerne testede calcipotriol på hudceller i laboratoriet og fandt ud af, at stoffet havde en positiv effekt på hudens cellevækst, ligesom vitamin D. Efterfølgende undersøgte de, hvordan calcipotriol blev nedbrudt i kroppen (metabolisme). Det viste sig, at calcipotriol blev hurtigt nedbrudt i leveren, uden at have toxistiske metabolitter, hvilket forhindre alvorlige bivirkninger. Figur 49 viser de metabolitter af calcipotriol, der blev identificeret.. Derefter fulgte en række dyreforsøg (in vivo) for at sikre, at calcipotriol havde den forventede effekt i en levende organisme. Forskerne gav rotter og minigrise radioaktivt mærket calcipotriol for at spore, hvordan stoffet blev metaboliseret. Dyreforsøgene bekræftede resultaterne fra laboratoriet.
Efter de lovende resultater fra dyreforsøgene begyndte kliniske studier på mennesker. Disse bestod af tre faser:
- Fase I – test på raske frivillige for at undersøge sikkerheden. Her blev det bekræftet, at calcipotriol ikke havde alvorlige bivirkninger.
- Fase II – test på en mindre gruppe psoriasispatienter for at vurdere effektivitet og dosering.
- Fase III – test på en stor gruppe patienter for endeligt at fastslå behandlingens effekt og sikkerhed.
Resultaterne viste, at calcipotriol markant forbedrede psoriasis uden alvorlige bivirkninger. Derfor kunne stoffet nu godkendes og markedsføres som en effektiv psoriasisbehandling.
8. Eksempel 2 - Fra diabetes til vægttab
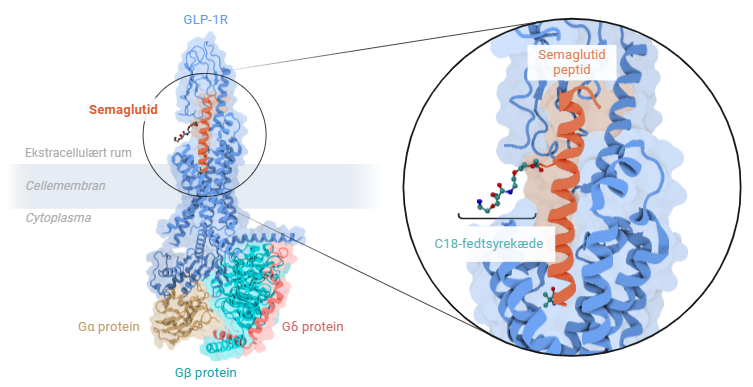
Semaglutid er det aktive stof i lægemidler, der bruges til behandling af type 2-diabetes og vægttab. Det virker ved at efterligne hormonet GLP-1 (glucagon-like peptide-1), som øger insulinproduktionen, reducerer appetitten og forsinker mavetømningen. Strukturen af semaglutid, bundet til en GLP-1 receptor, kan ses på figur 50. Semaglutid markedsføres under navnene Ozempic (til diabetes) og Wegovy (til vægttab).
Struktur af semaglutid
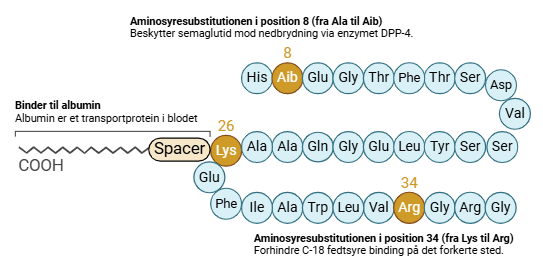
Semaglutid er en peptidbaseret GLP-1-analog, som består af 31 aminosyrer, næsten identisk med det naturlige GLP-1-hormon. Der er dog lavet følgende tre vigtige modifikationer, hvis samlede virkning forlænger semaglutids halveringstid, så det kun skal injiceres én gang om ugen. Figur 51, viser opbygningen af semaglutid.
- Aminosyreændring: Alanin er erstattet med Aib (α-aminoisosmørsyre) ved position 8, hvilket gør peptidet mere modstandsdygtigt over for enzymet DPP-4, der ellers hurtigt ville nedbryde det.
- Fedtsyremodifikation: En C18-fedtsyrekæde er koblet til, hvilket gør stoffet fedtopløseligt og forbedrer bindingen til proteinet albumin, som findes i blodet.
- Aminosyreændring: Lysin er erstattet med Arginin ved position 34, for at forhindre at C18-fedtsyrekæden binder til andet ed albumin.
Virkning
Semaglutid har længe været anvendt som det aktive stof i diabetesmedicin, men i de senere år har man opdaget, at en af bivirkningerne ved stoffet er, at det reducerer appetitten. Dette har ført til, at semaglutid nu også bruges til behandling af overvægt.
- Ved diabetes virker semaglutid ved at efterligne det naturlige hormon GLP-1, som hjælper med at regulere blodsukkeret. Det stimulerer bugspytkirtlen til at frigive insulin, når blodsukkeret er højt, samtidig med at det hæmmer frigivelsen af glukagon, som ellers ville øge blodsukkeret. Derudover forsinker semaglutid mavetømningen, hvilket giver en længere mæthedsfornemmelse og bidrager til mere stabilt blodsukker.
- Den appetitnedsættende effekt af semaglutid skyldes, at stoffet også påvirker hjernens appetitregulerende centre, hvilket gør, at man føler sig mæt hurtigere og i længere tid. Dette har gjort semaglutid til en populær behandling mod svær overvægt, hvor det kan hjælpe patienter med at opnå et betydeligt vægttab.
SNAC
Man har igennem mange år kun kunnet levere semaglutid som en injektion men ikke oralt i pilleform. Dette er grundet den høje enzymaktivitet (primært proteaser) i fordøjelsessystemet samt molekylets evne til at krydse cellemembraner. Da injektion er både dyrere og mindre behagelig for patienter, har der været et stort fokus på at overkomme disse udfordringer.
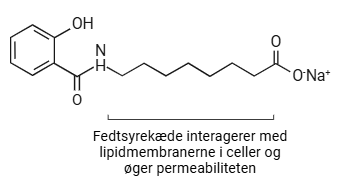
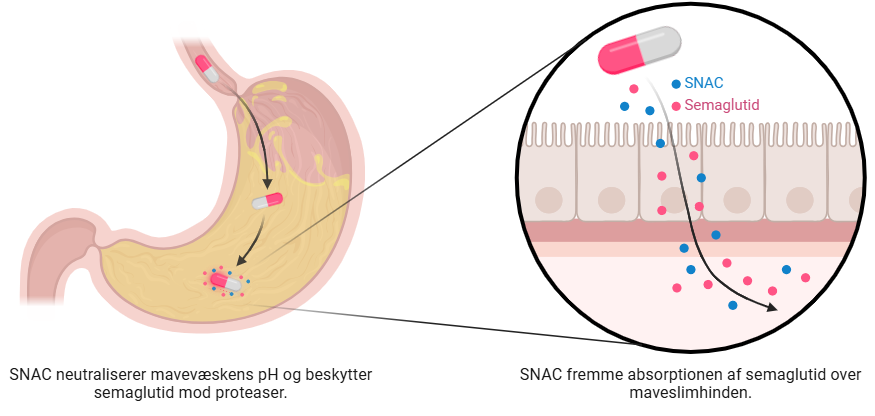
Til dette formål har man udviklet molekylet natrium N-(8-[2-hydroxybenzoyl]amino) caprylat (SNAC), hvis struktur er vist i figur 52. SNAC er i stand til at forbedre absorptionen af semaglutid i maven, neutralisere pH’en i maven samt beskytte det mod proteaser. SNAC bidrager dermed til at reducere nedbrydningen af semaglutid i fordøjelsessystemet og muliggør at semaglutid når systemisk cirkulation (blodbanen) mere effektivt, hvilket resultere i en øget biotilgængelighed. Dette har muliggjort, at <1% af semaglutid når GLP-1 receptoren, hvilket er tilstrækkeligt til at sikre en effektiv behandling gennem denne administrationsform, dog skal der bruges 100 gange så meget af det aktive stof, hvilket kan gøre at productionen kan have svært ved at følge med. Se illustration af, hvordan SNAC kan anvendes til oral levering af semaglutid i figur 53.
Interaktive øvelser
Det virtuelle laboratorium
Til dette undervisningsmateriale er der tilknyttet laboratorieøvelser i Det Virtuelle Laboratorium.
Her kan du prøve kræfter med udvikling af et lægemiddel mod psoriasis og eksperimentel genteknologi i et laboratorium, der er bygget op ligesom et professionelt bioteknologisk laboratorium!
Øvelserne tilknyttet “Lægemiddeludvikling” er: Lægemiddeludvikling.
Snak og byt
Aktiveringsenergi
Krig med bindinger
Krig med bindinger er en øvelse tilknyttet til undersiden 3: Organisk kemi og lægemidler. Formålet med øvelsen er at præsentere eleverne for intra- og intermolekylære bindinger og give et overblik over hvor stærke de forskellige bindinger er i forhold til hinanden.

