1. Udvikling af nye lægemidler
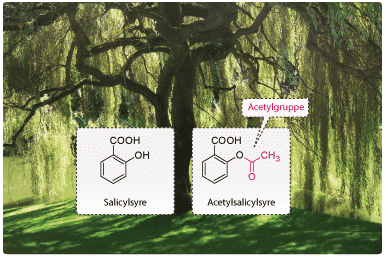
Et lægemiddel er et biologisk aktivt stof, som kan bruges til behandling af en sygdom eller bestemte symptomer. Lægemidler binder til biologiske targets i kroppen. Disse targets kan f.eks. kan være proteiner, sakkarider, nukleinsyrer eller lipider. Gode lægemidler virker specifikt og har derfor få bivirkninger. Lægemidler er som regel organiske molekyler, hvis strukturelle opbygning og sidegrupper har stor betydning for deres binding og effekt i kroppen.
At udvikle lægemidler er en stor udfordring, som ikke bliver lettere, når lægemidlet skal virke i hjernen. Hjernen er opbygget af komplekse neurale netværk, som benytter mange forskellige kemiske transmittersystemer, hvilket gør det kompliceret at forstå årsagen til sygdomme i hjernen. Hjernen er samtidigt svær at ramme, da den besidder en naturlig, selektiv barriere, som bestemmer, hvad der kommer ind og ud. Der går ca. 10 til 15 år, fra man får ideen til et lægemiddel, og til det er færdigudviklet. At være drughunter er en udfordrende opgave, som kræver megen viden om lægemidler, og om hvordan de virker.
Når nye stoffer opdages
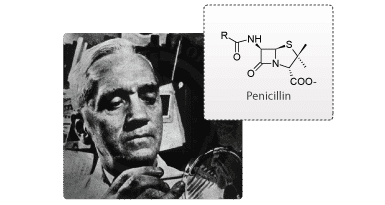
Tidligere i historien blev de fleste lægemiddelkandidater fundet tilfældigt. Et eksempel var, da Alexander Fleming i 1928 fandt ud af, at svampen Penicillium notatum producerede et stof, der effektivt slog bakterier ihjel. Penicillin revolutionerede måden, hvorpå man behandlede infektioner. Udviklingen af penicillin er bare et af mange eksempler på, hvordan svampe, planter, bakterier og dyr danner biologisk aktive stoffer, der kan bruges som lægemidler. I dag benytter de fleste medicinalvirksomheder, som bl.a. Lundbeck, sig af samme metode, dog på lidt anderledes vis.
Nye lægemiddelkandidater findes i dag ved at bruge store robotter, som screener kemiske biblioteker efter ”trial and error”-princippet. Ved en screening undersøges stofferne i de kemiske biblioteker for deres medicinske effekt på forskellige cellekulturer. Bibliotekerne kan både være tilfældigt syntetiseret med kombinatorisk kemi, eller kan være stoffer oprenset fra naturen. Som beskrevet tidligere er naturen rig på stoffer med biologisk aktivitet. Ved at screene kan mange stoffer hurtigt undersøges for deres bindingsegenskaber til biologiske targets. Nye potentielle lægemidler med de ønskede farmakologiske virkninger identificeres som hits. En enkelt screening giver tit flere hits, men der er stadig et stykke vej til et endeligt lægemiddel.
I dag laves der ofte en tredimensionel model, af den receptor eller det enzym, man ønsker at ramme med et lægemiddel. Dette kunne f.eks. være NMDA-receptorerne i hjernen. Disse receptorer har central betydning, når man behandler Alzheimers sygdom (se dropdown nedenfor). Ved hjælp af røntgenstrukturanalyse og kemiprogrammer til tredimensionel analyse kan forskerne modellere organiske molekyler på baggrund af viden om targets tredimensionelle struktur. Modellen kan bruges til at afprøve lægemiddelkandidater på target. Disse undersøgelser omtales ofte som in silico tests.
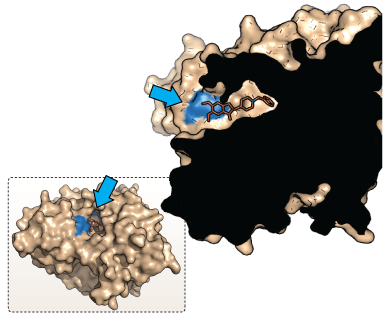
NMDA-receptoren
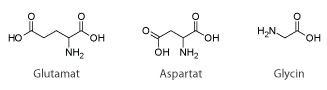
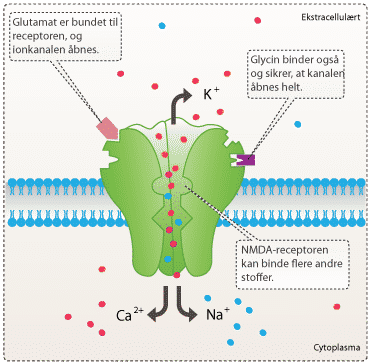
NMDA-receptoren har stor betydning for den excitatoriske neurotransmission i hjernen, hvilket betyder, at den er med til at forstærke signaloverførsel mellem nervecellerne i hjernen. Receptoren findes i nervesynapser, hvor den aktiveres, når glutamat bindes til den. Receptoren aktiveres af både glutamat og aspartat, men aspartat virker dog ikke lige så kraftigt som glutamat. Receptoren kræver desuden en co-agonist som glycin for at sikre en optimal åbning af receptorens ionkanaler. Glutamat er det primære excitatoriske neurotransmitterstof, som bruges i alle områder af hjernen. NMDA-receptoren er permeabel for Ca2+ ioner (se figur 6). Ca2+ strømningen igennem NMDA-receptorens ionkanal gør den helt speciel, da Ca2+ kan igangsætte mange forskellige processer i cellen. Forskere mener bl.a., at indstrømningen af Ca2+ er skyld i de molekylære ændringer, der har betydning for lagringen af langtidshukommelsen.
Hvordan virker lægemidler?
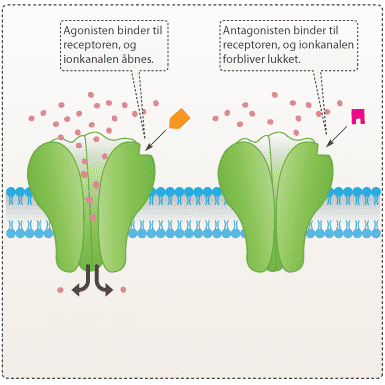
De fleste lægemidler påvirker helt bestemte biokemiske processer, som har indflydelse på, hvordan kroppens celler fungerer. Man designer ofte lægemidler med det formål, at den normale biologiske funktion påvirkes. Enten kan funktionen af det biologiske target nedsættes eller forbedres. Stoffer, der binder til en receptor og aktiverer receptoren, kaldes agonister (forbedre funktionen), mens stoffer, der hæmmer aktiveringen af receptoren, kaldes antagonister (nedsætter funktionen) (se figur 6). De fleste lægemidler virker som enten agonister eller antagonister.
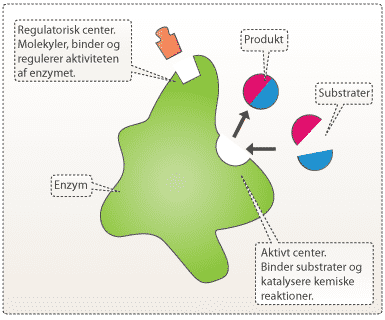
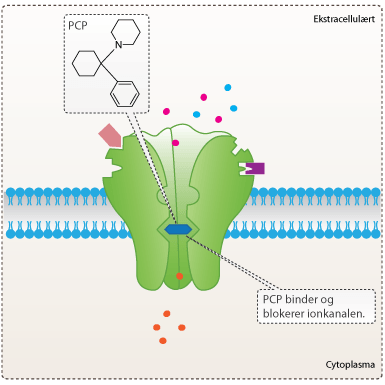
Da lægemidler tit ligner kroppens egne signalstoffer, skal de ofte konkurrere med disse om at binde deres mål (kaldet target). Hvis target er et enzym, kan lægemidlet f.eks. binde til enzymets regulatoriske center eller enzymets aktive center. Binding til det aktive center påvirker enzymet direkte, fordi det er her, de naturlige signalstoffer eller substrater binder og gennemgår den kemiske reaktion. Binding til det regulatoriske center kan derimod forårsage en ændring i enzymets tredimensionelle struktur (konformation), som indirekte ændrer formen af det aktive center. Det kan gøre, at signalstoffer eller substrater enten ikke kan binde sig, eller at de binder sig lettere end normalt. Hvis target er en receptor, vil lægemidlet ofte blokere de bestemte dele af receptoren, som binder signalmolekyler eller på anden måde har central betydning for receptorens funktion (se om NMDA- receptoren).
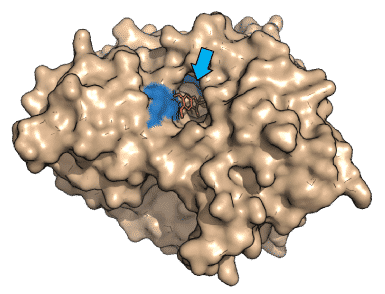
For at forstå, hvordan et lægemiddel binder til et enzym eller en receptor, er det vigtigt at kende til intermolekylære bindinger – altså kræfter mellem forskellige molekyler. Lægemidler designes til at binde specifikt til enzymer eller receptorer og kan fungere som enten agonister, antagonister eller inhibitorer. Antagonister hæmmer receptorer, mens inhibitorer hæmmer enzymer eller proteiner. Et andet centralt aspekt i lægemiddeldesign er isomeri. Du kan læse mere om disse emner – samt om thalidomid-skandalen, hvor man overså betydningen af isomeri – i de følgende dropdowns.
Struktur, intermolekylære kræfter og inhibering af et biologisk target
- Ion-dipolbinding: Stærke kræfter mellem en ion og en polært binding. Ionen tiltrækkes af den modsatte ladning af molekylets dipol.
- Hydrogenbinding: Bindingen mellem et hydrogenatom og oxygen (O), nitrogen (N) eller fluor (F) i ét molekyle til oxygen (O), nitrogen (N) eller fluor (F) i et andet molekyle. Bindingen kan f.eks. opstå mellem en NH-gruppe og en C=O-gruppe.
- Dipol-pipol binding: Tiltrækning mellem to polære molekyler, hvor de positive og negative ender vender mod hinanden.
- London binding (Van der Waals kræfter): Dette er en hydrofob vekselvirkning. Svage tiltrækningskræfter, der opstår midlertidigt mellem alle atomer og molekyler på grund af bevægelige elektroner. De er de eneste kræfter i ikke-polære molekyler.
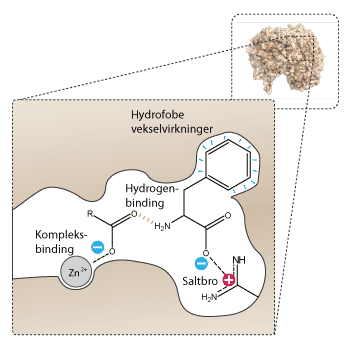
Lægemidlets mange bindinger til target gør den samlede binding mellem lægemidlet og target stærkt. Hvis target f.eks. er et enzym, findes der flere måder, hvorpå lægemidler kan hæmme de forskellige processer i cellen. Et stof, som kan hæmme en proces, kaldes en inhibitor. Lægemidler kan enten være reversible inhibitorer (ibuprofen) eller ikke-reversible inhibitorer (acetylsalicylsyre). Ikke-reversible inhibitorer forårsager kemiske ændringer og ødelægger target ved at binde sig covalent til target. Reversible inhibitorer danner mange svage bindinger til target, men forårsager ingen kemisk ændring. Bindingen er derfor reversibel – heraf navnet. Reversible inhibitorer bruges ofte som lægemidler, da de i langt mindre grad giver bivirkninger.
En inhibitor kan yderligere opdeles i tre kategorier: kompetitiv, non-kompetitiv (også kaldet ikke-kompetitiv) og ukompetitiv. Ved kompetitiv hæmning kan inhibitoren binde i det aktive center og kæmpe om pladsen med substratet. En kompetitiv inhibitor er reversibel og kan udkonkurreres ved tilførsel af mere substrat. En non-kompetitiv inhibitor binder til et andet sted på enzymet (allosterisk site), ændrer strukturen i det aktive center og forhindrer dermed substratet i at binde sig. En ukompetitiv inhibitor binder til enzym-substrat-kompleks, hvorved reaktionen blokeres og ikke kan fuldføres. En non-kompetitiv og ukompetitiv inhibitor kan ikke udkonkurreres af øget mængder substrat, men de er stadig reversible inhibitorer og kan fjernes ved f.eks. nedbrydning, temperatur- eller pH-ændringer.
Chirale lægemidler
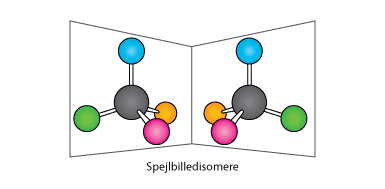
Et molekyle kaldes chiralt, når det indeholder et carbonatom, der er bundet til fire forskellige grupper. Dette carbon kaldes et chiralt carbonatom. For at finde ud af, hvilken form molekylet har, giver man de fire grupper en prioritet, alt efter hvilket grundstof de starter med. Gruppen med det højeste atomnummer i det periodiske system får højest prioritet, og den med det laveste får lavest prioritet. Når man har givet alle grupper en prioritet, vender man den lavest prioriterede gruppe væk fra sig selv, så man ser direkte på det centrale carbon og de tre andre grupper rundt om det. Hvis man derefter følger rækkefølgen fra højest til lavest prioritet og den går mod venstre, har molekylet S-form (S kommer af det latinske ord sinister, som betyder venstre). Går rækkefølgen i stedet mod højre, har molekylet R-form (fra rectus, som betyder højre på latin).
Et chiralt carbonatom kaldes også et stereocenter, og hvis et molekylet indeholder flere stereocentre, kan molekylet findes som flere stereoisomere. Stereoisomere kan enten være spejlbilleder af hinanden, hvor alle chirale centre er spejlbilleder, hvilket kaldes enantiomere. Eller kun nogle chirale centre er spejlbilleder af hinanden, hvilket kaldes diastereomere (se figur 11).
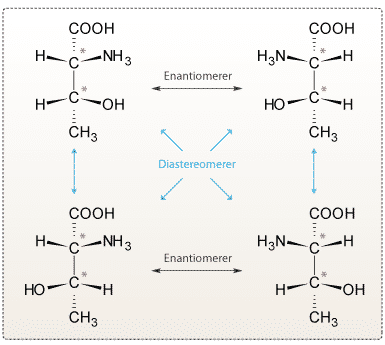
De fleste stoffer, der oprenses fra naturen eller fremstilles kunstigt i et laboratorium, har stereocentre. Det har vist sig, at det tit kun er en stereoisomer, som har den ønskede medicinske effekt. To forskellige stereoisomerer kan pga. deres forskellige strukturer virke på to fuldstændigt urelaterede receptorer, som hver især igangsætter to vidt forskellige biologiske processer (se dropdown om thalidomid-skandalen). Årsagen til dette er som omtalt orienteringen af de funktionelle sidegrupper (se figur 12).
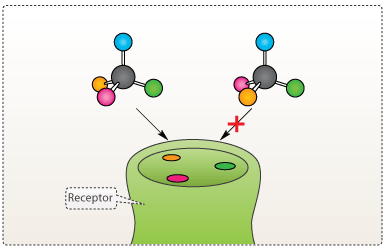
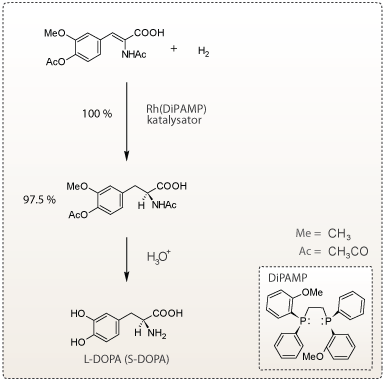
Betydningen af stereokemiske forhold i forbindelse med udviklingen af nye lægemidler har ført til, at der forskes meget indenfor fremstillingen af den rigtige stereoisomer med den ønskede medicinske virkning. I 2001 gik Nobelprisen i kemi til William Knowles og Ryoji Noyori for deres arbejde med fremstilling af stereoselektive kemiske synteser. W. Knowles fremstillede katalysatoren RhDiAMP, som bruges til syntesen af den ønskede stereoisomer af lægemidlet DOPA, som bruges til behandling af Parkinsons sygdom. Derved vil kun den ønskede stereoisomer af lægemidlet fremstilles.
Thalidomid-skandalen
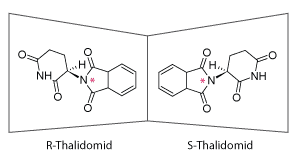
I 1956 blev Thalidomid lanceret til behandling af morgenkvalme og søvnbesvær hos gravide kvinder. I starten af 1960’erne blev der indrapporteret en lang række svære fødselsdefekter hos nyfødte som bl.a. manglende arme og ben. Det førte til, at den tyske producent Grünenthal i 1961 måtte fjerne lægemidlet fra hylderne. Skandalen skabte røre over hele verden og i 1968 indførtes et rapporteringssystem for bivirkninger i Danmark. Selvom skandalen ikke var årsag til opdagelsen af stereoisomere, havde den en væsentlig betydning for forståelsen af og opmærksomheden på stereoisomerers biologiske betydning i medicinalindustrien.
Lægemidlerne skal ramme deres molekylære mål i hjernen
Absorption
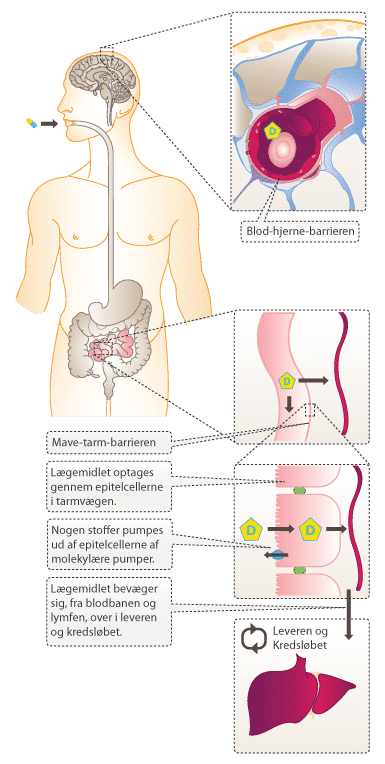
- Molarmasse skal være mindre end 500 g/mol.
- Stoffets lipofilicitetsfordelingskoefficent skal være mindre end 5. Log P < 5.
- Antallet af hydrogenbindingsdonorer skal være mindre end 5.
- Antallet af hydrogenbindingsacceptorer skal være mindre end 10.
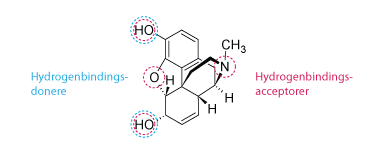
| Formel: | C17H19NO3 |
| Molarmasse (g/mol): | 285,34 |
| Log P: | 1,27 |
| H-donerer: | 2 |
| H-acceptorer: | 4 |
Distribution
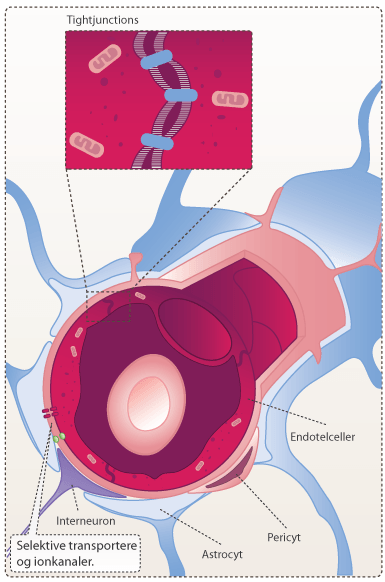
Stoffer, som optages gennem epitelcellerne i tarmen, bevæger sig hurtigt over i blodbanen. Det er dog ikke alle molekyler, som opløses i blodet. Upolære molekyler opløses ikke, men transporteres af forskellige transportproteiner. Fra blodbanen distribueres stoffet til leveren og derfra ud til de forskellige væv og organer. Et stof siges at være effektivt, hvis det rammer målorganet i tilstrækkelig koncentration. Visse dele af kroppen er dog særlig svære at nå. Dette er f.eks. tilfældet med centralnervesystemet (CNS). På trods af den gode blodgennemstrømning i hjernen, er den svær at nå med aktive lægemidler pga. blod-hjerne-barrieren (BBB for engelsk blood-brain-barrier). BBB er opbygget af endotelceller, som sidder meget tæt for at forhindre passage af stoffer mellem cellerne. Derved opretholder BBB et konstant ekstracellulært miljø i hjernen. Upolære substanser diffunderer over BBB forholdsvis uhindret, mens polære molekyler skal transporteres af specielle transportproteiner. Dog kan polære molekyler nemmere opløses i blodet.
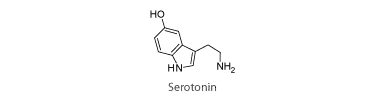
Neurotransmitteren serotonin har stor betydning for menneskers sindsstemning. Det har vist sig, at mange depressive har for lidt serotonin i hjernen. Serotonin er et eksempel på et stof, som ikke kan krydse BBB. Depression behandles derfor med alternative stoffer, som godt kan krydse BBB og dermed øge mængden af serotonin i hjernen. Disse stoffer kaldes SSRI-præparater.
Stofomsætning (metabolisme) og eliminering
De fleste stoffer nedbrydes i leveren af forskellige enzymsystemer, hvilket sker med forskellige hastigheder for de forskellige stoffer. Der findes stoffer, som i mindre grad end andre nedbrydes i leveren. Disse stoffer kaldes metabolisk stabile stoffer. Metabolismen af stoffer i leveren er en afgørende faktor, når nye lægemiddelkandidater skal udvælges, da nedbrydningshastigheden har stor betydning for stoffets effektivitet i kroppen. Stoffer, som omsættes for hurtigt i kroppen, egner sig ikke særlig godt som lægemidler, da de måske ikke når deres target i tilstrækkelig høj koncentration. Stoffer, der nedbrydes langsomt, kan ophobes, hvilket virker toksisk for kroppen.
Til sidst skal stoffet eller dets nedbrudte rester elimineres fra kroppen, hvilket kan ske gennem urin, afføring, sved, udånding med mere.
Test af lægemidler
Når forskere har identificeret en potentiel lægemiddelkandidat, påbegyndes en lang og grundig proces med at teste stoffet, både biologisk og kemisk. Indledningsvist udføres in vitro-forsøg, hvor stoffet undersøges uden for levende organismer – typisk i cellekulturer og med avancerede kemiske assays. Her forsøger man at besvare centrale spørgsmål som:
Hvordan trænger molekylet gennem biologiske membraner? Hvor fedtopløseligt og kemisk stabilt er det? Hvordan bliver det nedbrudt og udskilt fra kroppen? Og vigtigst: Er det giftigt?
Disse tidlige tests danner grundlaget for videre udvikling. De viser ofte, at det oprindelige molekyle skal ændres flere gange, før det har de rette egenskaber til at gå videre til test i levende organismer. De biologiske analyser in vitro foretages typisk i cellekulturer, og nogle af de mest anvendte celletyper beskrives i den første dropdown nedenfor.
Herefter følger en række prækliniske tests in vivo, hvor stoffets effekt og sikkerhed undersøges i forsøgsdyr – dette uddybes i anden dropdown. Til sidst, hvis resultaterne er lovende, kan lægemiddelkandidaten blive godkendt til test i mennesker, hvilket sker i fire veldefinerede kliniske faser. Disse gennemgås i den tredje dropdown.
Cellebaserede assays i præklinisk forskning
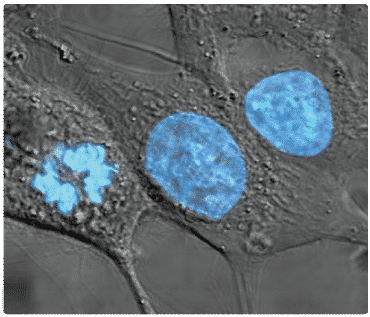
HeLa kræftcellerne bruges i dag i en lang række biomedicinske sammenhænge bl.a. for at undersøge bindingen mellem et potentielt lægemiddel og dets biologiske target. Cellerne stammer oprindeligt fra den 31-årige Henrietta Lacks, som i 1951 blev indlagt på Johns Hopkins Hospital med en cancer tumor. På trods af at hun døde få måneder efter, lever hendes tumorceller stadig i dag, hvor de bruges i mange forskellige biologiske assays. HeLa kræftceller omtales tit som udødelige, da de kan dele sig uendeligt mange gange.
Dyremodeller og prækliniske in vivo-tests
Efter en lang række in silico og in vitro tests er det tid til, at teste lægemiddelkandidaterne på levende organismer in vivo. Inden lægemidlet gives til mennesker, gennemtestes kandidatens effektivitet og toksikologi på forsøgsdyr. Der bruges mange forskellige slags forsøgsdyr, dog oftest mus og rotter. I Danmark kræver det godkendelse for at arbejde med forsøgsdyr. De enkelte forsøg skal også godkendes af Dyreforsøgstilsynet, som hører under Justitsministeriet.
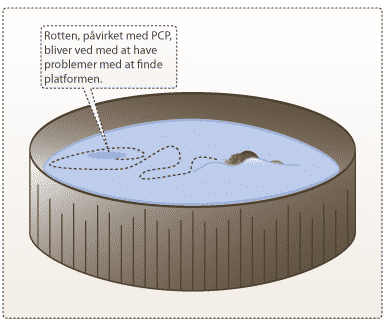
En af metoderne, der kan bruges til at undersøge et lægemiddels indvirkning på hukommelse og indlæring, er forsøg i Morris water maze (Morris vandlabyrint). Morris water maze ville kunne være relevant til test af lægemidler mod sygdomme som f.eks. Alzheimers sygdom og skizofreni, hvor der ses tab af hukommelse og indlæringsevne. I forsøget sættes en rotte i en stor vandtank fyldt med mælket vand. Under overfladen i den ene del af karret er der en lille platform, som giver rotten mulighed for at undgå at svømme. En normal rotte vil svømme rundt, indtil den finder platformen. Anden gang rotten bliver placeret i bassinet, vil den svømme direkte hen til platformen. I det ikke-normale tilfælde, som f.eks. ved hukommelsessvigt ved Alzheimers eller skizofreni, vil rotten have svært ved at huske placeringen af platformen og derfor svømme rundt uden at finde den hurtigt anden gang.
Kliniske faser og tests i mennesker
- Fase 1 (Sikkerhed): I første fase gives lægemidlet til en lille gruppe af raske frivillige (10 til 100 personer), og der igangsættes en undersøgelse af, hvordan den menneskelige organisme optager og reagerer på stoffet. I løbet af forsøget modtager forsøgspersonerne flere forskellige doser af stoffet. Dog meget mindre doser end en normal dosis, idet der holdes skarpt øje med tegn på forgiftning. I denne fase fokuseres der primært på, om lægemidlet har en giftig virkning i mennesket. Effektiviteten af stoffet evalueres ikke nødvendigvis.
- Fase 2 (Sikkerhed, effektivitet, dosering): I anden fase gives lægemidlet til en lidt større gruppe af frivillige (50 til 300 personer), som vil kunne have gavn af lægemidlet. Gennem denne fase undersøges forskellige doser for deres effektivitet og bivirkninger. Som regel udføres der sideløbende kontrolforsøg, hvor kontrolgruppen modtager placebo i stedet for det rigtige lægemiddel. Hverken forskere eller forsøgspersoner ved, hvilke grupper, der får hvad. Til sidst i forsøget sammenlignes doser og bivirkninger fra de to grupper, og de mest optimale doser bestemmes.
- Fase 3 (Sikkerhed, effektivitet, bivirkninger): I tredje og sidste fase udføres forsøg i stort omfang med mange frivillige (1500-4000 personer), som vil kunne have gavn af lægemidlet. Lægemidlet gives i de doser, som man tidligere har fundet passende. I løbet af forsøget går forsøgspersonerne til kontrol hos deres egen læge, hvor de rapporterer om bivirkninger. Denne undersøgelse giver mulighed for at se, om lægemidlet giver sjældne bivirkninger, dvs. bivirkninger hos nogle få af forsøgspersonerne.
- Fase 4: I denne fase er lægemidlet godkendt af myndighederne og vil nu kunne bruges til behandling af sygdommen. I denne fase laves der tit forsøg, hvor lægemidlet sammenlignes med allerede eksisterende behandlinger.

De meget omfattende undersøgelser, som skal udføres gennem de kliniske faser, gør det meget kostbart at udvikle lægemidler. Udviklingen af et nyt lægemiddel er estimeret til at koste omkring 800 mio. dollars. Selv om et lægemiddel kommer på gaden, kan det stadig blive taget af hylderne, hvis det ikke fungerer efter hensigten. Ligesom det var tilfældet med thalidomid. Efter endelig godkendelse og etablering på markedet holdes der altså stadig øje med nyopståede bivirkninger eller toksiske effekter.
2. Intro til hjernens fysiologi og funktion
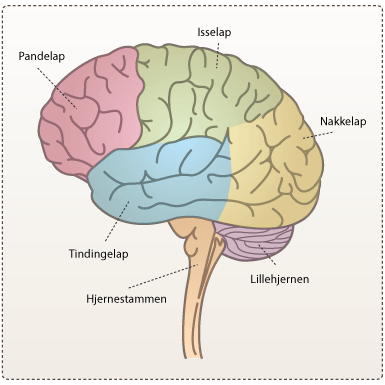
Centralnervesystemet (CNS) består af storhjernen (cerebrum), lillehjernen (cerebellum) og hjernestammen (truncus encephalicus). Hjernen er inddelt i to hemisfærer. Den venstre hemisfære fokuserer på detaljer (som et ansigt i en mængde), mens den højre del fokuserer på den brede baggrund (for at forstå placeringen i rummet). Den yderste del af hemisfæren kaldes cortex. Cortex er den del af hjernen, som bearbejder sensoriske indtryk og står for de kognitive funktioner som at tænke, huske og tage beslutninger. Cortex kan inddeles i fire lapper.
Pandelap (frontallap): Er den forreste del af hjernen. Den tager sig af bevidst tankegang, planlægning og organisering. Den varetager også store dele af hukommelse og opmærksomhed. Tillige har den stor betydning for vores følelsesliv.
Isselap (partietalap): Sidder bag frontallappen og står for opfattelsen af de forskellige sanseindtryk, smerte, berøring, tryk og temperatur, samt føle- og bevægefunktionen.
Tindingelap (temporallap): Denne del sidder under partietal- og frontallapperne. Denne del af hjernen tager sig af sanser som lugt, smag og hørelse. Ligeledes tager den sig af behandling og lagringen af hukommelse.
Nakkelap (baglap/occipitallap): Sidder i bageste del af hjernen lige over lillehjernen. Denne del opfanger og fortolker synsindtryk.
Lillehjernen (cerebellum) tager sig af de mest basale funktioner som balance, motorisk koordinering og muskelsamarbejde. Den er forbundet med resten af hjernen og modtager informationer fra øjne, ører og muskler. Lillehjernen har især betydning for vores finmotorik – f.eks. at gøre bevægelserne bløde. Lillehjernen står også for lagringen af motorisk lærte ting.
Det limbiske system – Den indre del af hjernen
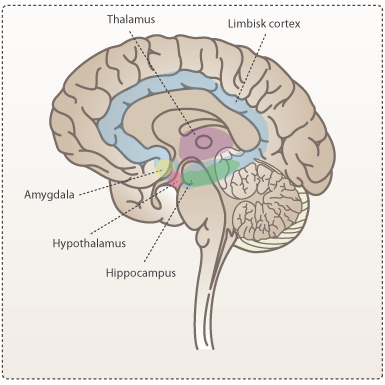
Det limbiske system (se figur 2) består af et stort antal neuroner, som fordeler sig til mange andre dele af CNS, f.eks. til pandelappen og mellemhjernen. Systemet varetager mange af hjernens funktioner som bl.a. indlæring og lagring af langtidshukommelse.
Amygdala er lokaliseret på den inderste del af tindingelappen og har betydning for følelseslivet og bearbejdelse af stærke følelser som f.eks. frygt. Amygdala kan påvirke området hypothalamus, som styrer frigivelsen af bl.a. stresshormonet adrenalin, hvilket giver et kropsligt respons som hjertebanken, øget svedproduktion og opmærksomhed. Amygdala har også betydning for de følelser, der tillægges oplevelser, inden de overføres til hukommelsen.
Hippocampus er ligesom amygdala lokaliseret på indersiden af tindingelappen og er vigtig for ind-læring og korttidshukommelse. Man mener også, at hippocampus står for overførelsen af korttidshukommelsen til langtidshukommelsen i andre dele af hjernen.
Thalamus ligger over hjernestammen og fungerer som et centralt omkoblingscenter for hjernens signaler. Den modtager og behandler forskellige typer information, især sensoriske signaler såsom syn, berøring, smag og hørelse. Thalamus bearbejder og omformer disse signaler, før de sendes videre til de relevante områder i cortex for videre fortolkning og bevidst opfattelse. Thalamus har samtidig central betydning for søvn og vågenhed.
Hypothalamus har mange nerveforbindelser og regulerer adskillige funktioner i kroppen. Området varetager eksempelvis funktioner som føde- og vandoptagelse. Hypothalamus kan igangsætte spise- og drikkeadfærd gennem forbindelser til cortex og thalamus. Området opretholder samtidig kropstemperatur og regulerer kroppens kemiske processer gennem et hormonsystem, der styrer hypofysen (hormonkirtel i hjernen lige under hypothalamus). Hypothalamus kontrollerer også kroppens indre ur.
Basalganglierne
Basalganglierne er en gruppe af kerner dybt i hjernen, der er vigtige for planlægning og kontrol af bevægelser. De hjælper med at igangsætte, koordinere og hæmme bevægelser, samt organisere signalerne til de forskellige muskelgrupper og sørge for, at de endelige motoriske bevægelser har den rigtige udformning. Basalganglierne findes i den indre del af storhjernen i begge sider og er områder, som består af flere dele, herunder striatum (nucleus caudatus og putamen), globus pallidus og substantia nigra.
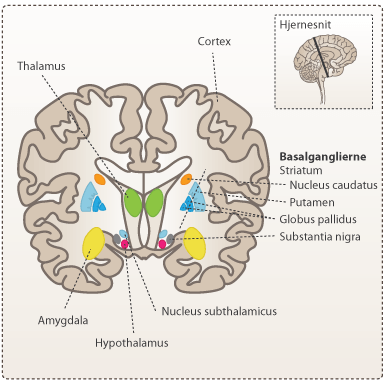
Substantia nigra (den sorte substans) sidder i midthjernen, placeret i begge hjernehalvdele. Den sorte substans spiller en central rolle i basalganglierne og dopaminsystemet. Området har derfor også betydning for kroppens motorik.
Striatum består af områderne nucleus caudatus og putamen. Området har forbindelse til og fra andre områder i basalganglierne ligesom andre områder i hjernen.
3. Alzheimers sygdom

Da Auguste døde, foretog Alois Alzheimer en obduktion af Auguste for, at undersøge hendes hjerne, og resultatet var slående. Områderne cortex, entorhinal cortex (hukommelse og rumlig orientering) og hippocampus (hukommelse og indlæring) bar tydelig præg af neurontab. I visse dele af hjernen manglede op mod en tredjedel af neuronerne, og i disse områder fandt Alois Alzheimer tynde aflejringer af, hvad han beskrev som en tæt sammenklumpet masse af nedbrudte celledele. De samme områder var samtidigt plaget af inflammation. I 1910 blev sygdommen kaldt ”Alzheimers sygdom” af Emil Kraepelin, som var en af Alois Alzheimers kollegaer.
Symptomer og diagnose
Alzheimers sygdom er en ud af flere former for demens, og sygdommen rammer typisk ældre personer. Sandsynligheden for at udvikle Alzheimers sygdom stiger med alderen. Ligesom Parkinsons sygdom er Alzheimers sygdom en neurodegenererende (nedbrydning og tab af neuroner) sygdom. Sygdommen forløber i tre stadier (tidligt, mellemliggende og sen), men starter som nedbrydning af nervecellerne i entorhinal cortex, hvorfra den spreder sig til hippocampus og amygdala (følelser og frygtrespons). Dette fører til en forstørrelse af hjernens væskefyldte områder kaldt hjerneventriklerne. Forstørrelserne kan ses allerede 10 til 20 år før patientens første symptomer. Aflejringerne spreder sig gennem hele hjernen, mens områderne skrumper. De primære symptomer på Alzheimers sygdom er tab af kognitive funktioner, forringelse af sprog og hukommelsesproblemer (se figur 2).
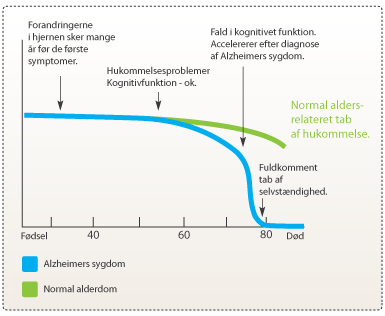
Diagnosen Alzheimers sygdom er svær at stille, da mange andre sygdomme skal udelukkes. Diagnosen bliver stillet på baggrund af en række neuropsykologiske tests og interviews, hvor lægerne spørger ind til patientens sygdomshistorie og forsøger at måle på patientens hukommelse. I Danmark benyttes forskellige spørgeskemaer og testskalaer (se figur 3).

Derudover udføres en række fysiske tests og laboratorieundersøgelser, hvor bl.a. patientens thyreoideahormon-niveau, B12-vitamin-niveau, leverfunktion og blodtal måles. Dette gøres primært for at udelukke andre sygdomme. Som tidligere beskrevet er Alzheimers sygdom karakteriseret ved indskrumpning af forskellige områder i hjernen. Hjernescanninger spiller derfor også en vigtig rolle i diagnosen af Alzheimers sygdom og er en god metode til at udelukke andre sygdomme. Her bruges især metoderne CT (Computed Tomography) eller MRI (Magnetic Resonance Imaging) (se dropdown om hjernescanninger). De forskellige tests udføres tit over en længere perioder, så lægerne kan holde øje med patientens hukommelse og symptomudvikling.
Hjernescanninger
Patologi
Alzheimers sygdom er ligesom Parkinsons sygdom karakteriseret ved, at visse dele af centralnervesystemet (CNS) undergår en degenerering. Den præcise årsag til at personer udvikler Alzheimers sygdom, er ikke fuldt klarlagt. De aflejringer Alois Alzheimer fandt i Augustes hjerne, var aflejringer af det tungt opløselige protein beta-amyloid (Aβ), som består af kun 42 aminosyrer. Akkumulationen og sammenklumpningen af proteinet har vist sig, at have en central rolle i sygdomsmekanismen for Alzheimers sygdom og dannelsen af de såkaldte senile plaques. Dette blev vist i løbet af halvfemserne, da forskere opsatte en model for Alzheimers i en transgen mus (se dropdown om transgene mus). Musen viste tydelige tegn på hukommelses- og indlæringsproblemer.
Transgene mus
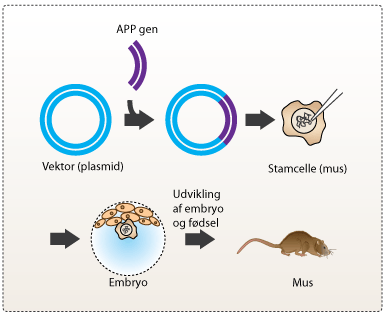
Man ved, at nogle mennesker udvikler senile plaques i hjernen i takt med, at de bliver ældre. Patienter med Alzheimers sygdom har dog ekstra mange senile plaques. Forskning har vist, at mutationer i genet som koder for APP, kan øge produktionen af beta-amyloid i hjernen. Dette hænger godt sammen med genetiske observationer hos patienter med Downs syndrom, som har tre kopier af APP genet, og som typisk udvikler en alzheimer-lignende tilstand, inden de bliver 60 år. Forskerne har en hypotese om, at sammenklumpningen af beta-amyloid til oligomere er farlig for cellerne, og at dannelsen af de større plaques måske er en forsvarsmekanisme, som beskytter neuronerne i hjernen mod de toksiske beta-amyloid oligomerer.
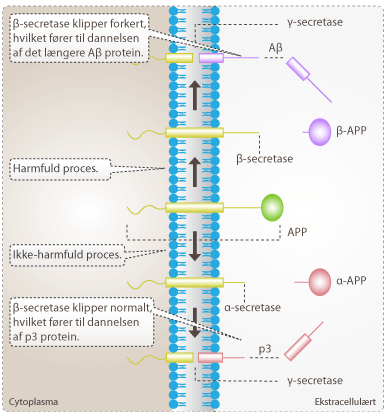
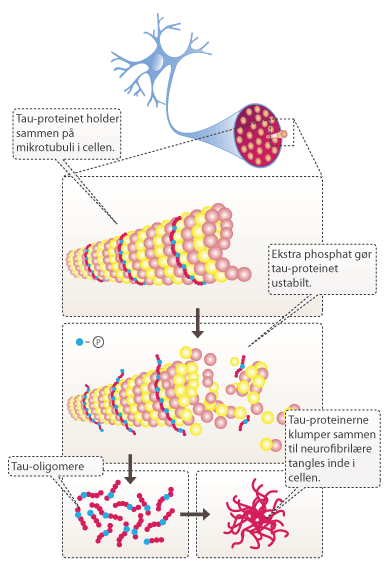
En anden ting, der karakterisere Alzheimers sygdom, er dannelsen af neurofibrillære tangles inde i hjernens nerveceller. De neurofibrillære tangles er sammenklumpninger af tau-proteinet, som i raske neuroner stabiliserer mikrotubuli. Mikrotubuli bruges til at transportere næringsstoffer gennem axonerne inde i nervecellerne og er en del af nervecellernes interne transportsystemer. Hos alzheimerpatienter er tau-proteinet hyperfosforyleret, og de enkelte tau-proteiner klumper sammen inde i neuronerne og ødelægger dem.
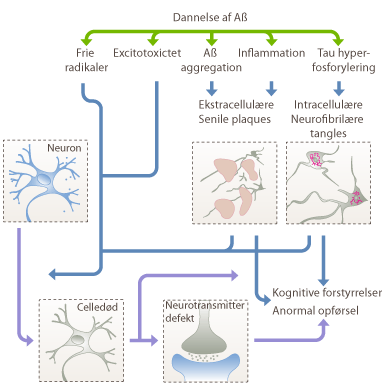
Akkumulationen af Aβ ødelægger neuronernes synaptiske kommunikation, ligesom at hyperfosforyleringen af tau-proteinet fører til ødelæggelse af nervecellerne. Alt sammen medfører forstyrrelser i flere af hjernens transmissionssystemer. I patienter med Alzheimers sygdom ses tit, at der er for meget af neurotransmitterstoffet glutamat. Den store mængde af glutamat kan medføre en tilstand, der kaldes excitotoxictet, hvor der ses en overdreven stimulering af de to glutamatreceptorer (NMDA og AMPA). Processen ødelægger nervecellerne, fordi cellerne optager ekstra mange calciumioner, hvilket sætter gang i processer, som medfører dannelsen af frie radikaler. Frie radikaler er ustabile og reaktive molekyler med uparrede elektroner. De kan skade celler ved at angribe DNA, proteiner og cellemembraner, hvilket bidrager til aldring og sygdomme som Alzheimers.
Udviklingen af medicin mod Alzheimers sygdom
Ginkgo biloba kaldes også tempeltræet, da man i det gamle Kina havde træet stående foran de store buddhistiske templer. Træet har været kendt for dets medicinske egenskaber i årtusinder i Østen. I den buddhistiske tro var træerne hellige, og man troede, at de var med til at holde mennesker sunde og raske. I 1970’erne havde historien om Ginkgo biloba spredt sig til Vesten, hvor det blev muligt at købe ekstrakt fra træet i form af kosttilskud og naturmedicin. Opdagelsen af Ginkgo biloba satte gang i en masse undersøgelser af træets medicinske virkninger. I dag findes der et hav af medicinske artikler om Ginkgo biloba. Mange af disse artikler peger mod at Ginkgo biloba har en effekt på hjertet og det arterielle kredsløb. Nogle studier af Ginkgo biloba har også vist, at ekstrakt fra bladene kan have en lettere virkning på patienter med Alzheimers sygdom, mens andre studier viser det modsatte.
I nyere forskning undersøges effekten af ekstrakt fra Ginkgo biloba i mus med humane Alzheimers-gener. Studier tyder på, at ekstraktet kan hæmme sammenklumpningen af beta-amyloid i hippocampus og fremme dannelsen af nye nerveceller, hvilket kan forbedre kognitive funktioner. Kombinationsstudier som undersøger Ginkgo biloba ekstrakt med andre midler bl.a. docosahexaensyre (DHA) viser også lovende resultater med reduktion af neurodegeneration. Selvom disse fund er positive, er der stadig behov for yderligere kliniske forsøg for at bekræfte effekten hos mennesker.

Acetylcholinesterase
Der findes ikke nogen behandling, der kan helbrede Alzheimers sygdom. Medicinen, der findes i dag, kan kun bruges til behandling af symptomerne på Alzheimers sygdom, og på den måde udskyde sygdommen. Der forskes derfor fortsat meget i Alzheimers sygdom. Der søges efter metoder, der kan udvikle mere effektive behandlingsformer. Acetylcholin er en neurotransmitter, der spiller en central rolle i nervesignal overførsel. Den er vigtig for hukommelse, læring og muskelkontrol. I Alzheimers sygdom falder niveauet af acetylcholin, hvilket bidrager til kognitive problemer. Forskning inden for området har vist, at mængden falder, fordi de acetylcholinproducerende nerveceller ødelægges. Acetylcholin nedbrydes desuden naturligt af acetylcholinesterase (AChE) i nervecellernes synapsekløfter, nogle Alzheimers patienter kan have forhøjet mængde af AChE, hvilket skaber en ekstra mindskning af acetylcholin i hjernen.
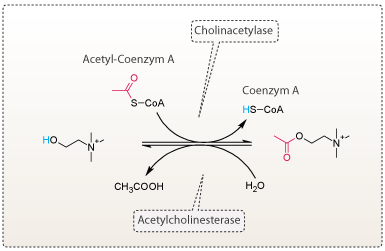
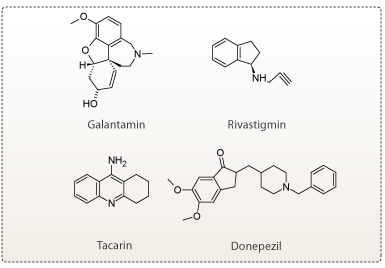
De første lægemidler, der blev udviklet til behandling af Alzheimers sygdom, var derfor rettet mod acetylcholinesterase. Lægemidlerne virkede ved at hæmme acetylcholinesterase, og forhindre nedbrydelse af acetylcholin (se figur 9). De mest brugte acetylcholinesterase inhibitorer i dag er: donepezil, tacrin, rivastigmin og galantamin.
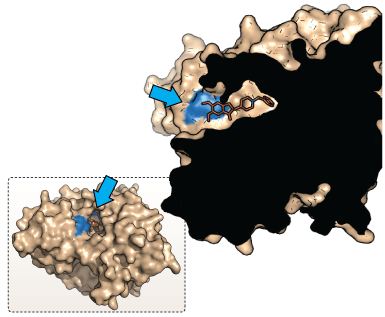
NMDA-receptoren
Som tidligere beskrevet har neurotransmitterstoffet glutamat vist sig også at have stor betydning for udviklingen af Alzheimers sygdom, da overdrevne mængder af glutamat kan medføre excitoxitet, en proces, hvor nerveceller skades eller dør på grund af overstimulering af neurotransmitteren. Forskere udviklede derfor lægemidlet memantin, som er en ikke-kompeditiv antagonist til NMDA-receptoren. Lægemidlet virker ved at forhindre strømmen af Ca2+ gennem ionkanalen på NMDA-receptoren. Derved forhindres den fatale dannelse af frie radikaler i hjernen. Behandlingen af patienter med både memantin og acetylcholinesterase inhibitorer har i en række studier vist sig at forbedre forløbet for patienter med Alzheimers sygdom.
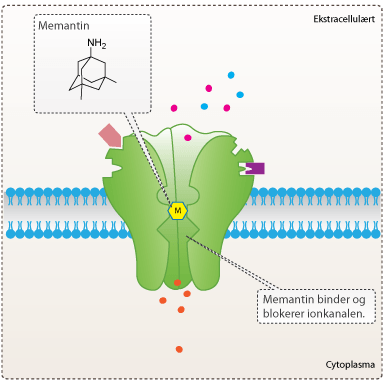
Memantin er i dag godkendt, og bruges til behandling af patienter med moderat til svær Alzheimers sygdom, som er det tredje og sidste stadie i sygdomsforløbet. Memantin virker specifikt og har relativt få bivirkninger, der omtales som ufarlige. De mest almindelige bivirkninger er: hovedpine, svimmelhed, omtågethed og hallucinationer. Den nuværende medicin til behandling af Alzheimers sygdom kan holde sygdommen i skak i et eller flere år, mens patienter, som ikke behandles medicinsk, udvikler demens i løbet af ganske få måneder til år.
Syntesen af Donepezil
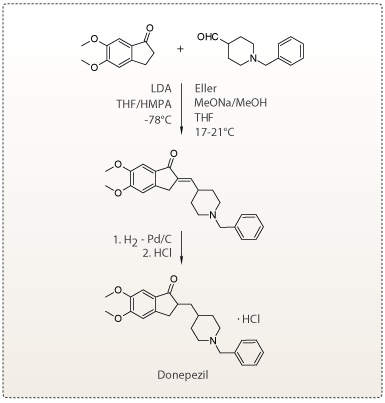
4. Parkinsons sygdom

Symptomer og diagnose
Parkinsons sygdom er en kronisk neurologisk lidelse, som typisk rammer personer i 55-60 års alderen. Sygdom er neurodegenererende og er karakteriseret ved mangel på neurotransmitterstoffet dopamin i de områder af hjernen, som styrer musklerne. Med sygdommen følger en lang række symptomer, hvor de mest dominante er ukontrollerede rystelser (tremor), langsomme bevægelser (hypokinesi), stivhed i musklerne (rigiditet), balancebesvær og problemer med finmotorik. Nogle patienter oplever en særlig svær grad af motorisk invalidering og har derfor problemer med helt basale funktioner som at tale, at styre afføring, synke og holde balancen. Ud over de motoriske symptomer lider mange parkinsonpatienter også af søvnløshed og ca. 50% oplever perioder med depression. Sygdommen har desuden vist sig at kunne medføre demens og anden påvirkning af patientens kognitive funktioner som f.eks. dømmekraft.
Diagnosen Parkinsons sygdom stilles klinisk på baggrund af sygdomshistorie og forskellige fysiske undersøgelser. Lægerne kan også bruge laboratorietests eller hjernescanninger, hvis der er tvivl om, hvorvidt symptomerne skyldes andre sygdomme som f.eks. lægemiddelinduceret parkinsonisme eller atypisk parkinsonisme (parkinsonisme plus). Disse to sygdomme deler nogen af symptomerne med Parkinsons sygdom, men er forårsaget af andre faktorer. Den bedste indikator for om patienten har Parkinsons sygdom, er at afprøve lægemidlet L-DOPA (se fokusboks om L-DOPA) på patienten og se, om der sker en mindskning af symptomerne.
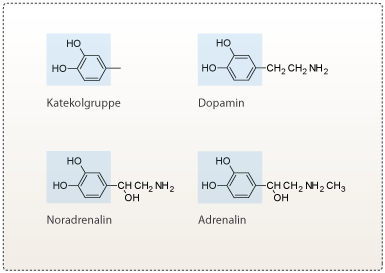
L-DOPA omdannes til dopamin i hjernen
Neurotransmitterstoffet dopamin dannes normalt ud fra aminosyren tyrosin (se figur 2). L-DOPA er et lægemiddel, som bruges til at øge mængden af dopamin i hjernen hos patienter med Parkinsons sygdom. L-DOPA kan passere blod-hjerne-barrieren og blive optaget i centralnervesystemet, hvor det hurtigt omdannes til dopamin. Det er ikke muligt at behandle direkte med dopamin, da neurotransmitterstoffet ikke kan krydse blod-hjerne-barrieren. L-DOPA gives som oftest sammen med andre lægemidler, som kaldes COMT inhibitorer. COMT inhibitorer hæmmer nedbrydningen af L-DOPA, inden det når hjernen.
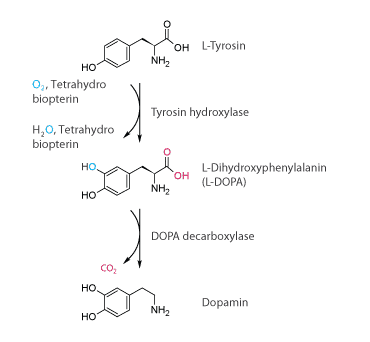
Patologi
Forskere er gennem de seneste 50 år begyndt at få en bedre forståelse af, hvad der forårsager Parkinsons sygdom. Parkinsons sygdom er ligesom Alzheimers sygdom karakteriseret ved, at visse dele af centralnervesystemet (CNS) nedbrydes. Specielt i det hjerneområde, som kaldes substantia nigra, sker der en betydelig nedbrydning af de nerveceller, som producerer neurotransmitterstoffet dopamin. Nervecellerne i dette område er en del af et indviklet netværk i basalganglierne, hvor de kommunikerer med flere andre områder. Disse tætte forbindelser har betydning for afviklingen af bevægelser. Sammen med neurotransmitterstofferne acetylcholin og glutamat indgår dopamin i en fin balance, hvor de tre neurotransmitterstoffer sammen styrer og finjusterer muskelkontraktioner. Ved en frivillig bevægelse bruges glutamat til at sende eksitatoriske signaler fra cortex til thalamus og tilbage til motorisk cortex (se figur 5). Disse signaler finjusteres, ved op- og nedregulering, i basalganglierne. Basalganglierne har stor betydning for udformningen af de frivillig bevægelse, da området regulerer og koordinerer hæmningen af forskellige motoriske systemer.
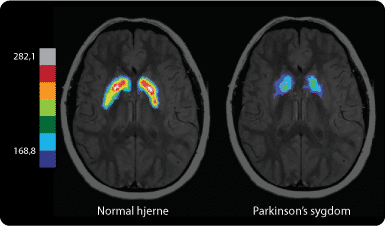
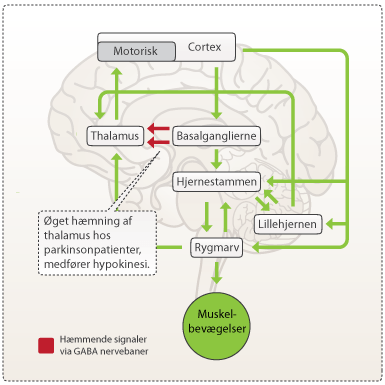
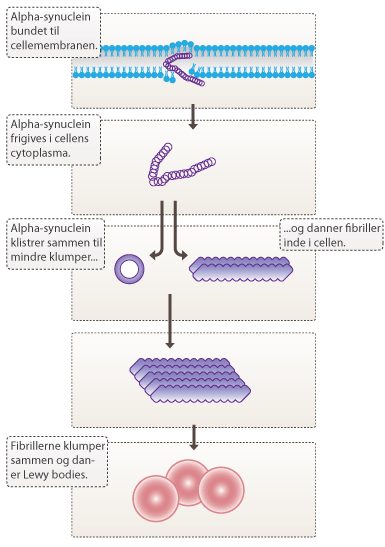
Der forskes intensivt i årsagerne til, at de dopaminproducerende celler i substantia nigra ødelægges. Den generelle opfattelse er, at det både er genetiske og miljømæssige faktorer, som spiller ind. En ting, der i høj grad karakteriserer Parkinsons sygdom, er dannelsen af lewy bodies i hjernen. Lewy bodies er unormale klumper af protein, som findes inde i neuronerne hos de fleste parkinsonpatienter. De udgøres af mange forskellige sammenfiltrede proteiner heriblandt alpha-synuclein og ubiquitin.
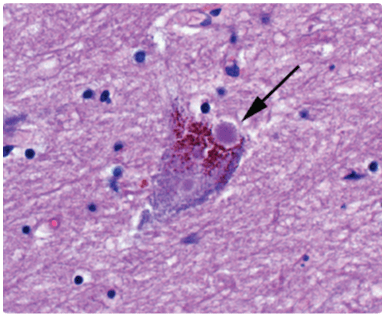
I 2000 lavede forskerne Chen og Feany en model for Parkinsons sygdom i Drosophila melanogaster, som på dansk kaldes bananfluen. Ved hjælp af bioteknologi indsatte de genet som kodede for alpha-synuclein. Undersøgelsen viste et progressivt tab af de dopaminproducerende neuroner i fluerne, ligesom man fandt klumper af alpha-synuclein. På trods af de opklarende resultater i bananfluer, har forsøg med mus ikke vist tegn på Parkinsons sygdom. Forskere er derfor i tvivl, om det er synucleinklumperne, som er toksiske, eller om de er en foranstaltning mod for meget af det frie synuclein, som måske er toksisk. Hvad der præcis forårsager neuronernes ødelæggelse, er derfor ikke klart.
Lewy bodies er ikke kun begrænset til substantia nigra, men kan også findes i mange andre, ikke-motoriske, dele af hjernen som cortex og amygdala . Forskere mener, at det kan være årsagen til at mange af de ikke-motoriske symptomer på Parkinsons sygdom. Proteinsammenklumpninger ses også i andre sygdomme som Alzheimers sygdom og Downs syndrom. Forskning har også vist, at dannelsen af frie radikaler og funktionsfejl i cellernes kræftværker, mitondrierne, kan have en central betydning for sygdomsmekanismen i Parkinsons sygdom.
Udvikling af medicin til behandling af Parkinsons sygdom
Symptomerne på Parkinsons sygdom var allerede kendt for mere end 4500 år siden og blev kaldt Kampavata. Dengang brugte man bønnerne fra planten Mucuna pruriens til behandling af symptomerne. Bønnerne fra denne eksotiske plante indeholder naturligt små mængder af stoffet L-DOPA. Brugen af Mucuna pruriens bønner, som på dansk kaldes fløjlsbønner, til behandling af Parkinsons sygdom er den ældst kendte behandlingsmetode . Forskere fik derfor også hurtigt ideen til at behandle sygdommen ved at øge mængden af dopamin i hjernen. Man begyndte derfor at give L-DOPA til patienterne, og L-DOPA er i dag forsat lægemidlet, som har den mest dæmpende effekt på parkinsonsymptomer.

Virkningen af L-DOPA aftager dog over en forholdsvis kort periode på ca. 5 år, og lægemidlet medfører ofte mange bivirkninger som f.eks. muskelkramper og ufrivillige bevægelser. Der kommer derfor løbende nye farmaceutiske strategier til behandling af Parkinsons sygdom. De fleste ny strategier forsøger at øge mængden af dopamin i de relevante områder af hjernen.
Cigaretter, fed mad, alkohol og kaffe – en ny behandling af Parkinsons sygdom?
MAO-hæmmere
En af strategierne, som bruges til at øge mængden af dopamin i hjernen, er de såkaldte MAO-inhibitorer. MAO-inhibitorer virker ved at blokere det aktive center på enzymet MAO. MAO-inhibitorer bruges også i stor grad til behandling af depression.
Hugh Blaschko var i 1930’erne en af de første, der interesserede sig for MAO-enzymet, og det var da også ham, der navngav stoffet. Det var dog først i slutningen af 1960’erne, at man fandt ud af, at MAO-enzymet ikke var et enkeltstående enzym, men at der faktisk eksisterede to eller flere enzymer, som havde forskellige substrater. Det var en stor opdagelse, da man snart fandt ud af, at MAO A og B også var distribueret forskelligt i hjernen. F.eks. fandtes MAO B primært i basalganglierne . Dette åbnede muligheden for de specifikke MAO-hæmmere, som ikke gav så mange bivirkninger.
I 1972 udviklede Knoll og Magyar en irreversibel MAO B-inhibitor, l-deprenyl, som var yderst specifik. Den virkede dog ikke særlig effektivt på depressive patienter. Det var først da Peter Reiderer var på udkig efter en MAO B-hæmmer til brug i behandlingen af Parkinsons sygdom, at l-deprenyl blev fundet frem. De første kliniske forsøg var overbevisende, og l-deprenyl blev hurtigt en del af behandling mod Parkinsons sygdom i Europa, hvor stoffet blev givet med L-DOPA som supplement. Dette viste sig at give bedre overlevelse for patienterne. l-deprenyl blev dog først godkendt 15 år senere som selegilin i USA af FDA.
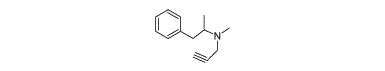
Rasagilin virker ved at binde sig covalent til coenzymet FAD, og forlænge sig ind i det aktive center på enzymet.
MAO B-inhibitorer har ligesom andre lægemidler også bivirkninger. Bivirkningerne varierer fra lægemiddel til lægemiddel. Men de mest almindelig bivirkninger er:
- Hovedpine
- Dyskinesier, dvs. ufrivillig bevægelser
- Influenzalignende symptomer, kvalme, svimmelhed, nedsat appetit, feber og vægttab
Alternativ behandling af Parkinsons sygdom
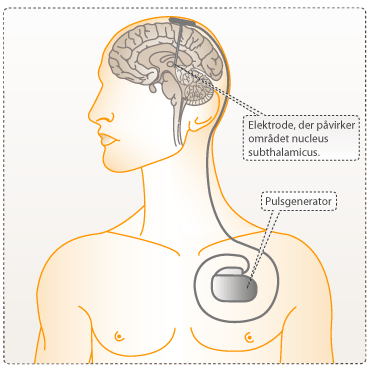
Syntesen af L-DOPA
Forskning i ny og forbedret behandling
Der forskes i dag intenst i at finde nye og bedre lægemidler til behandling af Parkinsons sygdom. Ligeledes er forskere begyndt, at få nye ideer til behandlinger. Således er genterapi og stamcelleterapi også kommet på tale.
5. Skizofreni

Symptomer og diagnose
Skizofreni er en neurologisk lidelse i hjernen. Sygdommen ændrer den skizofrenes tanker og opførsel. Sygdommen rammer begge køn og udvikler sig typisk i 15-30 års alderen. Skizofreni kan ses som et tab af grebet om virkeligheden. Der findes mange symptomer på skizofreni, men de fleste kan inddeles i to grupper, som kaldes positive symptomer (psykotiske symptomer) og negative symptomer (grundsymptomer). Ud over de to grupper af symptomer oplever 75-80% af de skizofrene også kognitive problemer som problemer med koncentration, hukommelse, indlæring og organisering.
Positive symptomer
De positive symptomer viser sig hovedsagligt i perioder med psykoser. Symptomerne viser sig i form af vrangforestillinger, hallucinationer (både visuelle og auditive), samt uorganiseret tale og opførelse. De mest almindelige hallucinationer er auditive, hvor den skizofrene hører stemmer. Stemmerne opfattes som regel som ondsindede. Det kan f.eks. være en person, der kritiserer eller kommenterer den skizofrenes gøren og laden. De mindre almindelige hallucinationer er de visuelle, hvor den skizofreni ser ting, som ikke er der. Hallucinationer giver den skizofrene en følelse af forfølgelse, ubehag og angst.
Vrangforestillinger viser sig hos en skizofren som urealistiske forestillinger om omverdenen. Forestillingerne stemmer ikke overens med virkeligheden. Eksempler kan være, at han eller hun har AIDS, eller at efterretningstjenester som CIA har opsat overvågningsudstyr for at holde øje med den syge.
Negative symptomer
De negative symptomer kan ses som den skizofrenes mangel på normale mentale træk. De negative symptomer ses typisk i perioderne mellem psykoserne. De viser sig ofte som:
- Følelsesforstyrrelser og følelsesmæssig nedtoning (mangel på ansigtsudtryk og kropssprog)
- Mangel på energi, motivation og initiativ
- Ingen følelse af glæde – følelsesmæssig ambivalent
- Autistiske symptomer – trække sig ind i sig selv, opsøger ikke social kontakt
- Katatoniske bevægelser – pludselig stivnen, unaturlige bevægelser, gentagende bevægelser
Diagnose
I Danmark bruger man ICD-10 klassificeringssystemet til at diagnosticere skizofreni. Klassifikationssystemet er udviklet af WHO og bruges i en lang række lande til at tolke symptomer og til at diagnosticere den rigtige type af skizofreni eller af andre sygdomme. Her nævnes tre former for skizofreni.
- Paranoid skizofreni er den mest almindelige form for skizofreni og er kendetegnet ved vrangforestillinger, som begrænser sig til et bestemt emne. I filmen ”A Beautiful Mind” hjemsøges den geniale matematiker John Nash af flere forskellige personligheder. Han driver ud i troen om, at USSR skjuler koder i magasiner og aviser, og at det er hans opgave at bryde koderne for Pentagon. John Nash er et eksempel på typisk paranoid skizofreni med både visuelle og auditive hallucinationer og vrangforestillinger.
- En anden form for skizofreni er Hebefren skizofreni, som karakteriseres ved uorganiseret tankegang og handlinger uden mål. Den skizofrene har svært ved at forstå omgivelserne og kan pludselig bryde ud i latter, som hverken hænger sammen med situationen, eller med hvad der bliver sagt. Denne form for skizofreni debuterer typisk i løbet af puberteten eller de tidlige voksenår.
Katatonisk skizofreni er karakteriseret ved abnorme bevægelser og stillinger, som kan blive ved i timevis. Den skizofrene er stille og taler kun sparsomt – ligesom han eller hun ikke reagerer på henvendelse.
Patologi
At forstå den biologi, som ligger bag skizofreni, er stadig en meget stor udfordring for forskerne. Skizofreni involverer mange af de tanke-, adfærds- og følelsesmønstre, som gør os til mennesker. Det er derfor også svært at sætte fingeren præcist på det, der forårsager sygdommen.
Der er mange faktorer, som har vist sig at spille ind på udviklingen af skizofreni. Det er f.eks. vist, at skizofreni er arveligt betinget (se figur 2) . Hvis din enæggede tvilling har skizofreni, er der 48% chance for, at du selv udvikler sygdommen. Den nyeste forskning inden for skizofreni har vist, at sygdommen skyldes en ustabilitet i nogle familiers arvemasse. Forskere har fundet en række mutationer i gener spredt ud over kromosomerne. Disse mutationer kan associeres med skizofreni. På trods af dette er der stadig et stykke vej til, at man med en gentest kan undersøge babyer for risikoen for senere i livet at udvikle skizofreni. De genetiske faktorer vejer tungt, men i studier af enæggede tvillinger har man fundet ud af, at begge tvillinger ikke nødvendigvis var disponerede for at udvikle skizofreni, på trods af at enæggede tvillinger deler alle gener. Årsagen til dette er, at miljøet også spiller en central rolle i udviklingen af skizofreni. Psykosocialt stress i barndommen eller traumatiske begivenheder i løbet af livet kan forårsage skizofreni . Helt præcist anslås det, at skizofreni er 80% arveligt betinget og 20% miljøbetinget.
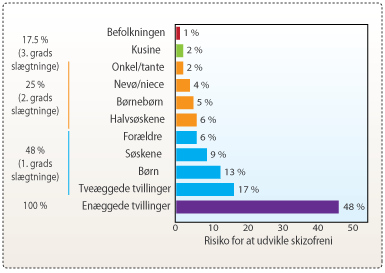
Forskere er kommet på sporet af, at der sandsynligvis er fejl i flere af hjernens transmittersystemer, og det kan være årsagen til sygdommen.
Dopamin- og NMDA-receptor-hypoteserne
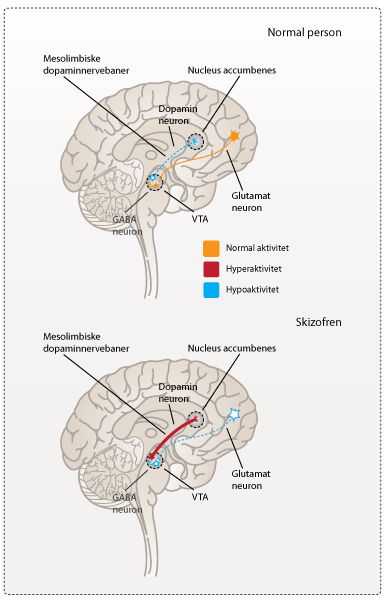
Dopaminhypotesen er den ældste og har eksisteret de sidste 30 år. Hypotesen opstod da amfetamin og kokain ledte forskere på sporet af, at hjernens belønningssystem kunne være involveret i skizofreni. Man vidste, at både amfetamin og kokain forbedrede neurotransmissionenen med katekolaminer (se figur 3) i hjernen. Stofferne udløste signaler fra det ventrale tegmentale område (VTA) og frigav dopamin i nucleus accumbens. Større mængder amfetamin kunne give brugeren en overdosis, som medførte psykotiske tilstande, der lignede de positive symptomer, som man kender fra skizofreni. Forskerne mente derfor, at for meget dopamin i belønningssystemet i forhold til dopaminreceptorer, kunne være årsagen til skizofreni.
Et andet spor var stoffet PCP (phenycyclidin). PCP var et nyt bedøvelsesmiddel, som blev introduceret i 1950’erne. Forsøg med stoffet gjorde dog flere af testpersonerne paranoide, og gav dem hallucinationer. Man valgte derfor at droppe brugen af PCP. Bivirkningerne af PCP havde ligheder med flere af de positive og negative symptomer, som man kendte fra skizofreni. PCP virker på glutamatsystemet ved at blokere NMDA-receptorer ne. Bivirkningerne ved brugen af PCP ledte til en hypotese om, at NMDA-receptorerne var mindre aktive og derfor ikke i samme grad kunne regulere signaltransmissionen med dopamin i belønningssystemet (se figur 4).
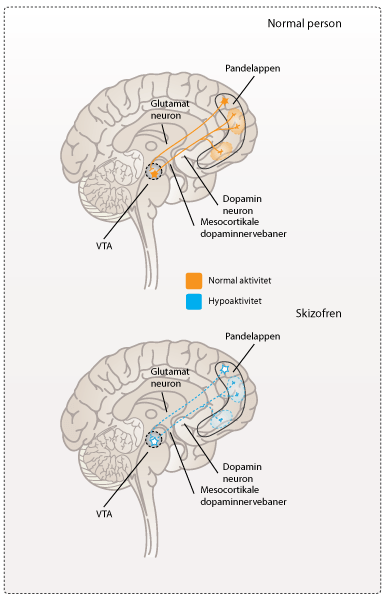
Forskere mener, at hypotesen om de mindre følsomme NMDA-receptorer også kan forklare de negative symptomer i skizofreni. Glutamat virker normalt fremmende på dopaminneuronerne, som strækker sig fra VTA til pandelappen. Nedsat følsomhed i NMDA-receptorerne vil medføre en nedsat aktivitet af disse dopaminneuroner (se figur 4). Hypotesen om nedsat aktivitet af NMDA-receptorerne underbygges af de mutationer, som forskere har fundet i gener hos skizofrene. Disse mutationer menes at kode for gener som har betydning for neurontransmission i glutamatsynapserne og specielt gennem NMDA-receptorerne.
Sygdommen skizofreni involverer sandsynligvis flere af hjernens transmittersystemer og signalveje. Den manglende forståelse af patofysiologien bag sygdommen betyder, at man ikke kan kurere skizofreni, men kun behandle symptomerne. Ligesom man tilsvarende kun kan behandle, ikke helbrede, smerter i ryggen på patienter med kronisk dårlig ryg.
Skizofreni og selvmedicinering
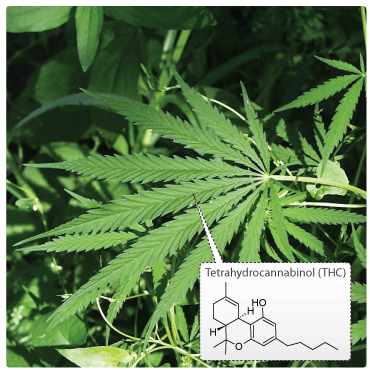
Mange skizofrene patienter misbruger forskellige former for euforiserende stoffer som hash og alkohol. Denne form for selvmedicinering, som det populært kaldes, er ikke nogen behandling af sygdommen, men kan i mange tilfælde forværre de psykotiske symptomer og forlænge perioder med psykoser. Ca. 20% af de skizofrene misbruger enten alkohol eller hash. Hos nogen starter misbruget før psykosen, hos andre efter. Det er vist, at alkohol og hash i større mængder stimulerer dopamin, serotonin og noradrenalin og kan derfor forværre/fremkalde psykoser. F.eks. virker det aktive stof i hash, THC (Tetrahydrocannabinol), ved at øge mængderne af dopamin i nucleus accumbenes. Ligeledes mener lægerne dog, at hash muligvis indeholder andre stoffer, som kan virke antipsykotisk.
Mange skizofrene misbruger også andre stoffer som amfetamin, benzodiapiner eller hårdere stoffer som kokain. Brugen af euforiserende stoffer kan fastholde og forværre den psykiske lidelse hos den skizofrene.
Udvikling af medicin til behandling af Skizofreni
Skizofreni behandles med antipsykotika, som modvirker psykotiske symptomer. Den første generation af medicin, som blev udviklet til behandling af skizofreni, koncentrerede sig primært om dopaminsystemet og kaldes typisk antipsykotika. Det første antipsykotiske stof, chlorpromazin, blev ved et tilfælde opdaget i 1950’erne under en række kliniske undersøgelser af et nyt antihistamin (lægemidler mod allergiske reaktioner) . Chlorpromazin var tænkt som et middel til behandling af høfeber. I forsøget deltog en lang række testpersoner. En af disse personer var skizofren. I perioden mens forsøget stod på, forsvandt flere af testpersonens positive symptomer. Dette bekræftede betydningen af dopaminsystemet. Chlorpromazin virker ved at hæmme D2-dopaminreceptorerne, som findes i cortex, det limbiske system og striatum.
Chlorpromazin var udgangspunktet for de lægemidler, der efterfølgende blev udviklet til behandling af positive symptomer hos skizofrene. Haloperidol var et af disse lægemidler. Stoffet bandt 100 gange bedre til D2-receptoreren end chlorpromazin. Den stærke effekt af lægemidlet hæmmede dopaminens virkning så godt, at det gav flere af patienterne parkinson lignende symptomer, pga. dopamins virkning i den motoriske neurotransmission fra substantia nigra til striatum.
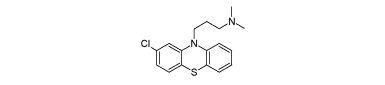
Anden generation af antipsykotika
For at forbedre effekten af lægemidlerne og fjerne de parkinsonlignende bivirkninger begyndte man, at tænke i nye baner. Det har i løbet af de sidste 10-20 år førte til andengeneration af lægemidler til behandling af skizofreni. Disse lægemidler kaldes også atypisk antipsykotika. Den nye generation virker stadig som antagonister på D2-receptoren, men de hæmmer ikke i lige så høj grad som de tidligere lægemidler. Samtidig har den nye generation af stoffer også en hæmmende virkning på flere af de andre neurotransmittersystemer i hjernen. Sertindol og clozapin er eksempler på andengenerationsstoffer. Begge har effekt på både dopamin-, noradrenalin- og serotoninsystemerne.
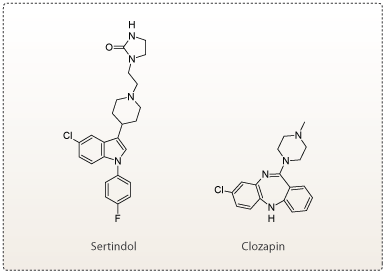
Man har længe vidst, at neurotransmitteren serotonin havde betydning for følelser og humør . Det var opdaget gennem erfaringer ved brug af lægemidler til behandling af depression. Men den multiple virkning af lægemidler var på det tidspunkt en ny måde at udvikle antipsykotiske lægemidler på. De nye antipsykotiske lægemidler er effektive mod positive symptomer, og forskellige studier har vist, at de måske også har en virkning på kognitive og negative symptomer. Samspillet mellem serotoninsystemet, dopaminsystemet og de nye antipsykotikas multiple virkningsmekanismer er endnu ikke velbeskrevet.
Antipsykotiske stoffer har ligesom andre lægemidler også bivirkninger. Disse opstår, fordi stofferne blokerer dopaminssystemet for kraftigt, eller fordi de influerer på andre systemer end dem, som har betydning for skizofreni. Bivirkningerne varierer fra lægemiddel til lægemiddel. Men de mest almindelig bivirkninger er:
- Ekstrapyramidale symptomer (EPS): Parkinsonsymptomer: tremor, muskelstivhed, kramper
- Tørhed i munden, sløret syn, svimmelhed
- Bedøvende virkning
- Øget vægt
- Forøgelse af hormonet prolaktin
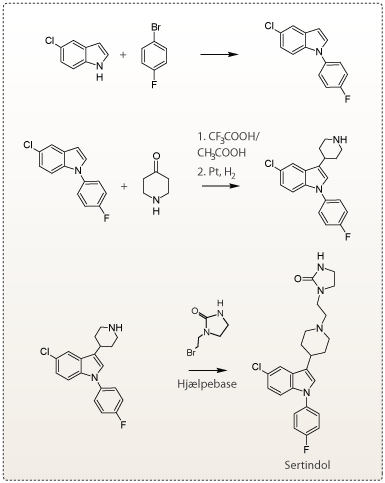
Syntesen af Sertindol
6. Posterdesign
Opbygning af poster og præsentation
At præsentere naturvidenskabelig forskning er ikke altid lige nemt. Derfor bruges ofte plakater, såkaldte posters, til at fremvise forskning på f.eks. messer eller konferencer. Her kan du finde tips og tricks til, hvordan du laver en god poster.
Oversigt
1. Meningen med en poster
2. Indhold
3. Layout
4. Skrifttype
5. Tekst og farver
6. Grafik
7. Formater
8. Programmer
9. Inspiration
Meningen med en poster
En plakat, eller det der på engelsk kaldes en poster, bruges i videnskabelige kredse til at præsentere forskningsresultater. I det følgende vil der blive givet en række retningslinjer til, hvordan du kan lave en god poster til præsentation af din forskning, ide, projekt eller lignende.
Posterens fornemste opgave er at fortælle om din forskning kort og præcist. Posteren fungerer altså som en opsummering af dit arbejde. Den skal kunne læses på 5 min af alle inden for målgruppen.
Når du skal til at lave din poster, er det i første omgang vigtigt, at du tænker på, hvad det er du gerne vil fortælle med din poster. Du skal altså definere meningen med posteren. I den forbindelse kan det være en god ide at prøve at finde en historie, en rød tråd, så man har et naturligt fortælleflow i posteren. På den måde vil læseren i høj grad blive guidet fra begyndelse til slutning, hvilket gør dit videnskabelige arbejde lettere fordøjeligt.


Indhold
Posteren skal i høj grad indeholde de samme elementer som en hver anden præsentation af videnskabeligt arbejde. Det vil sige, at der i stor udstrækning findes de samme afsnit som i f.eks. en rapport eller i en videnskabelig artikel, dog meget kortere. At være kortfattet og præcis i sin formulering er yderst vigtigt, når man arbejder med posteren som præsentationsform, da man let ”drukner” i tekst. Et eksempel på afsnit til din poster kunne være:
1. Titel og navn
Overskriften på posteren må gerne være lidt chatchy, det er det første læseren ser og bør derfor være spændende for at fange opmærksomhed. Under titlen står oftest navnet på forfatteren(e) samt evt. kontaktinformationer.
2. Introduktion
Her gives kort baggrunden for projektet. Det kan ofte være en fordel, hvis introduktionen afsluttes med en problemstilling, da det leder naturligt videre til problemformuleringen.
3. Problemformulering eller målet med posteren
Hvad er det, man gerne vil undersøge.
4. Materialer og metoder
Eller ofte bare metode bruges til at beskrive, hvilke metoder der er brugt til at opnå resultaterne.
5. Resultater
Beskriver de opnåede resultater. Her er det igen vigtigt at være meget restriktiv i sin formulering, da dette afsnit ofte bruger meget plads på posteren. Det er vigtigt kun at medtage de vigtigste resultater. Ofte vil du/I selv være til stede ved posterpræsentationen og kan på den måde forklare om yderligere resultater, hvis det skulle være nødvendigt.
6. Diskussion og konklusion
Her diskuteres og konkluderes på resultaterne. Diskussionen kan også præsenteres i forbindelse med resultaterne, det kommer an på, hvad der giver det bedste overblik. I sådanne tilfælde skal konklusionen selvfølgelig i et afsnit for sig selv.
7. Referencer
Stort set alt videnskabelig forskning bygger på anden forskning, og det er her vigtigt at kreditere de respektive forskere. Det kan være svært at vide, hvornår man skal referere, og hvornår man ikke behøver det. Som tommelfingerregel bør man altid referere til andre, hvis det, man hævder, ikke er alment kendt. Et simpelt eksempel kunne være: ”Proteiner har primær, sekundær, tertiær og kvarternær struktur ”, hvilket er alment kendt og behøver derfor ingen reference. Dog er ” Enzymet β-galactosidase i E. coli indeholder 1023 aminosyrer” ret specifikt og bør understøttes med en reference.
Layout
En af de vigtigste egenskaber for en poster er et godt layout. Men hvad er et godt layout? Det er et layout, der hjælper med til at forklare det budskab, man gerne vil fortælle med sin poster. Under tilblivelsen af posteren kan det ofte være svært at bevare overblikket, hvorfor det i mange tilfælde kan være en god ide at lave en håndtegnet skitse først. Brug gerne 10 minutter på at lave nogle hurtige skitser, som kan diskuteres, således at den underliggende struktur for posten er på plads, før det faktiske arbejde på computeren starter. Skitsen sikrer også, at alle i gruppen har en ide om, hvor man er på vej hen, så der ikke opstår misforståelser. Skitsen er selvfølgelig ikke universel og ændres næsten med garanti mange gange undervejs i processen, men danner altså et godt udgangspunkt, når man starter på posteren.
Da posteren til forskel fra for eksempel en bog er helt åben, er det vigtigt at guide læseren i den rækkefølge, man ønsker, posteren skal læses. Dette kan gøres med eksempelvis grafiske elementer som billeder eller anden grafik, men en simpel nummerering kan også virke til formålet.
De enkelte elementer
Skrifttypen, eller det der på engelsk kaldes en font, er meget vigtig for hvor let læselig og indbydende posteren bliver. Normalt læses en poster på ca. en meters afstand, og brødteksten bør derfor ikke være mindre end 20-24 punkter. Overskrifter skrives typisk med en skriftstørrelse på mellem 100- 120 punkter. Referencer og kontaktoplysninger kan skrives mindre (14-20 punkter), da de kun er relevante for den meget interesserede læser, som virkelig vil nærstudere posteren.
Normalt bruger man skrifttyper med fødder, når man laver brødtekst, men på postere kan andre let læselige skrifttyper også bruges, da teksten er så relativt stor, så behovet for fødder er mindre. På figuren herunder kan du se forskellige skrifttyper.

Tekst og farver
Det vigtigste ved teksten på en poster er, at den er letlæselig. Dette opnås lettest, hvis der er stor kontrast mellem farven på teksten og baggrunden. Dette betyder oftest i praksis, at brødteksten reelt kun kan have en farve, nemlig sort. Dermed ikke sagt at eksempelvis en mørk blå ikke kan bruges på en lys baggrund, men i de fleste tilfælde fås det bedste resultat med sort på hvidt eller lys baggrund.

Farvevalget på en poster er også yderst vigtigt. Farverne på en poster bør som udgangspunkt være relativt afdæmpede, så de ikke stjæler fokus fra det udførte videnskabelige arbejde, som posteren skal formidle. Dog kan der benyttes stærke farver til at lægge særlig vægt på enkelte elementer som f.eks. en særlig vigtig graf eller figur.
Grafik
To af de vigtigste elementer i en poster er grafik og billeder. I denne kategori falder illustrationer, grafer, tabeller og billeder, der skal være med til at beskrive din forskning. Det er som med alt andet på en poster vigtigt, at du kun medtager det, som er absolut nødvendigt for, at du kan fortælle din historie. Når du laver grafik til din poster, er det vigtigt, at du overvejer, hvilken kvalitet du skal bruge. Grafikken skal have en høj nok opløsning til at blive skalleret op på eksempelvis en A0 side (841×1189 mm). Dette betyder typisk at det materiale, der findes på nettet, ikke er i god nok kvalitet, men det er umiddelbart svært at se. Grunden hertil er, at computerskærmen ofte kun kan vise 72 dpi (dots per inch), mens et papirprint ofte skal bruge mellem 200-300 dpi for at se ordentligt ud. Anvender man billeder eller grafik, som ikke er i god nok opløsning, kommer det til at se således ud:
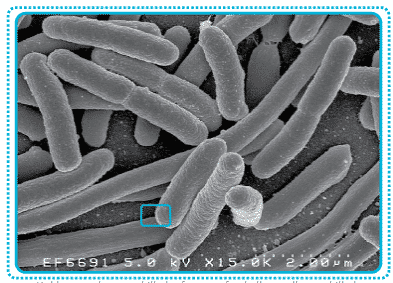
Formater
Hvilket format du vælger at benytte, er helt op til dig. De mest gængse størrelser er den internationale A-størrelse, som de fleste måske kender i form af A4 papiret. Her kan downloades en PDF med alle A- størrelser, som kunne være relevante. Det mest brugte format er A0 (841x1189mm), men også A1 og A2 kan bruges til postere.
Hvorvidt der benyttes landskabs- eller portrætorienteret papir er helt op til jer/dig, men det kan ofte være en fordel at bruge landskabsorienteret papir, da det føles mere naturligt at kigge på.
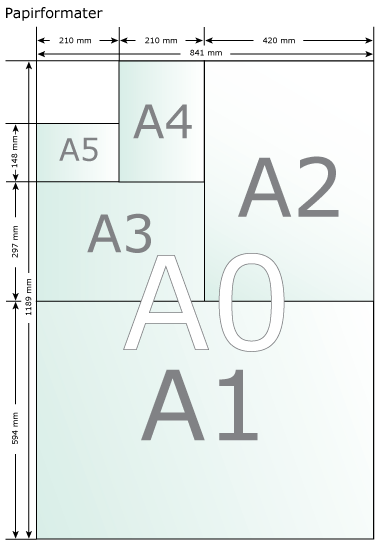
Her kan du hente predefinerede posterformater til PowerPoint:
(gem ved at højreklikke og vælge “gem destination som”)
PowerPoint: A1 og A0
(skabelonen er landskabsorienteret, denne kan ændres under fanen design -> slide orientering)
Programmer
Når en poster skal designes, er det vigtigt, at man bruger de programmer, man føler sig godt tilpas i. Det nytter altså ikke noget at bruge programmer, som man først skal til at lære at bruge for så derefter at skulle designe sin poster. Ydermere er det en stor fordel at bruge programmer, som benytter vektorgrafik. Grunden hertil er, at man her kan skalere alt grafik fra eksempelvis A4 til A0 uden tab af kvalitet, forudsat at alt er indsat/lavet som vektorer selvfølgelig.
Eksempler på programmer, som benytter vektorgrafik, er PowerPoint og Publisher fra Microsoft, men også mere avancerede programmer som Illustrator eller Indesign fra Adobe kan med fordel bruges til formålet. Har man først lært at bruge eksempelvis Illustrator, bruger man aldrig andet, da de fleste funktioner fungerer langt bedre end i f.eks. PowerPoint.
Tips: For at undgå at posteren ændrer sig, når du overfører den til print, kan det være en god idé at konvertere den til PDF. Dette kan gøres ved at gemme som PDF i de fleste nyere programmer, men ellers findes der konverteringsværktøjer på nettet.
Inspiration

Udover disse relativt simple eksempler kan der findes inspiration fra andre gymnasieelever eller DTU-studerende. Når posteren er færdig, skal den oftest præsenteres. Til dette kan du på følgende links finde ti gode råd til, hvordan du laver en god mundtlig præsentation, og hvordan du laver en god posterpræsentation, begge på engelsk.
God fornøjelse med at lave din poster!
PS: Hvis du ikke kan konvertere til PDF på andre måder, kan du bruge denne online server:
Gratis online pdf konvertering (vær opmærksom på at der kan forekomme kvalitetsforringelser ved denne metode)
Postere fra DTU studerende
Herunder kan du se en række eksempler på postere lavet af DTU studerende.

Posteren er lavet i forbindelse med faget “Design af bio- og miljøteknologisk processer”, hvor civilingeniør studerende indenfor både miljø- og bioteknologi i grupper skulle etablere en fiktiv virksomhed. Præsentation af virksomheden skete bl.a. ved en posterkonference. Vores virksomhed, PowerSeed, præsenterer her, i form af en poster, fordelene ved vores afgrøder, som er genetisk optimeret til produktion af 2. generations bioethanol. Lavet af Mads Bonde og Hans Genee.

Posteren er lavet i forbindelse med en bachelorprojekt med titlen ”Platform for High-Throughput Screening of Microorganisms by Using Flux And Image Analysis”. Målet med projektet var at udvikle et hurtig screeningsplatform for cellekulturer, ved at bruge et nyt udviklet billedanalyse software. Dette software skal kunne måle vækst og produktivitet af et given kemikalie. Samtidig udviklede vi en ny metode til at få detaljeret information om cellens metabolisme ved at anvende flux analyse. Dette bruges til at afgøre hvilke gener er essentielle for at opnå en effektiv “cellefabrik”, derved sænke produktionsomkostninger til at producere nye produkter i mikrobielle celler. Projektet er udført af Melanie Khodaie.
Posteren er lavet som en del af faget “Comparative Microbial Genomics: A Bioinformatics Approach” Målet med projektet var at undersøge forskellige Pseudomonas aeruginosa genomer for en række gener som er ansvarlige for nitrogen fikseringen i disse organismer. Posteren blev præsenteret ved en poster session hvor den fik en plads både på baggrund af videnskabeligt så vel som designmæssigt indhold. Projektet er udarbejdet af Rune T. Nordvang, Søren Damkiær, Rune Jensen og Nicholas Jochumsen. Hent en stor eller lille version af posteren i pdf.
Postere fra Unge Forskere
Posters lavet af unge forskere fra 2008
A Novel Process to Highly Improve the Bioethanol Production
Jeg deltog med denne poster i forbindelse med verdensmesterskabet for unge forskere; Intel ISEF, hvor 20 millioner unge er med i opløbet. Posteren repræsenterer en lille del af et halvt års arbejde, hvor jeg var ansat på Novozymes og arbejdede med omdannelsen af restproduktet DDGS til bioethanol, protein og energi. Den originale poster anvendt ved konkurrencen havde intet Novozymes logo, da dette strider mod regler til ISEF.
Lavet af, student fra Lyngby Tekniske Gymnasium, Christoffer Norn på Novozymes.
Udforskning og udnyttelse af sonoluminescens
Posteren er lavet i forbindelse med deltagelse i den internationale del af Kinas Unge Forskere konkurrence CASTIC. Projektet er vores afsluttende Teknologi opgave i 2.g på HTX Ishøj og omhandler omdannelsen af lyd til lys ved udforskning af spontan kavitation ved bobler i et medium under påvirkning af et lydfelt – Sonoluminescence. Ved fænomenet sonoluminescence kan f.eks. små luftbobler opnå en meget høj temperatur og herved lyse.
Lavet af Magnus Maduro Nørbo og Nicklas Juel Pedersen, Ishøj HTX.
Kemisk syntese af Ferrofluid
Poster til den nationale kinesiske konkurrence for unge forskere, CASTIC. Projektet er lavet i forbindelse med en eliteordning på Lyngby Tekniske Gymnasium, og handler om hvordan man optimerer den kemiske fremstilling af magnetiske væsker, de såkaldte ferrofluids. Ferrofluids er suspenderingen af magnetiske nanopartikler i en væske, som så agerer magnetisk.
Lavet af Michael Schantz Klausen, TEC Lyngby HTX.
Antimikrobielle Peptider
Posteren er lavet til Unge Forskere finalen i Århus. Projektet er lavet på Institut for Systembiologi på DTU og var en del af mit studieretningsprojekt i 3.G. Projektet er om antimikrobielle peptider og muligheden for at de kan blive en del af en ny generation af antibiotika, der kan erstatte de gamle og efterhånden ineffektive antibiotikum. Denne poster er en ud af i alt fire posters, og en del af teorien bag projektet er beskrevet her.
Lavet af Cecilia Engel Thomas, Ordrup Gymnasium.
Plakat om Mikrobiologiens Centrale Dogme
Vi kendet det alle, Det Centrale Dogme, en af grundstenene indenfor biologi og bioteknologi. Men læring behøver ikke være kedeligt, og tager man de rigtige briller på, kan de processer en celle er i stand til at udføre, være meget inspirerende og vilde.
Hans Jasper Genee fra Biotech Academy, har udviklet en plakat, der viser Mikrobiologiens Centrale Dogme, så alle kan se hvor inspirerende og spændende det er, samt hvor detaljerede og vilde ting alle celler på jorden er i stand til.
På plakaten ses processen fra DNA, til RNA, til protein, alt tegnet virkelighedstro i forholdet 1:25.000.000. Desuden er der på plakaten små tekster og skematiske tegninger, hvis nu man bare skal vide mere om hvad der foregår.
Klik på plakaten for at se den i stor størrelse.
Print plakaten og hæng den op på dit værelse, i din klasse, i biologilokalet eller andre steder hvor der mangler et kreativt indslag, der ikke kun er lærerigt, men også er super sejt at kigge på.
Hør mere om hvordan plakaten blev til: Her kan du se en lille film med Hans, der fortæller hvordan det har været at lave en plakat om det centrale dogme, og hvorfor kreativitet og forskning går hånd i hånd..


