Proteiner som drug targets
For at udvikle et nyt lægemiddel er det nødvendigt at have viden om den sygdom, der skal behandles, samt det target, der skal rammes. Et target kan være mange forskellige biomolekyler, men i langt de fleste tilfælde er det et protein. Derfor er det vigtigt at have en grundig forståelse af proteiner og deres funktion for at kunne designe et specifikt lægemiddel, der kan interagere med target.
Der findes mange forskellige proteiner, hvoraf enzymer, receptorer og transportproteiner er særligt vigtige, da de udgør langt de fleste targets for de lægemidler, vi kender i dag. Udover proteiner findes der også andre typer drug targets, såsom DNA og RNA.
Uanset hvilket target der påvirkes, kan brugen af lægemidler føre til konsekvenser såsom udvikling af tolerance og afhængighed.
Enzymer
Et enzym er et protein, som fungere som en katalysator for biologiske processer. Enzymer kan ikke få reaktioner, der normalt ikke vil forløbe, til at ske, men de kan øge reaktionshastigheden i begge retninger for reaktioner, der vil normalt vil forløbe men virker ved at sænke aktiveringsenergien så en ligevægt indstille sig hurtigere, uden at påvirke hvor ligevægten er eller selv at blive forbrugt under processen, se figur 3.
Ligesom andre proteiner, består enzymer af af aminosyrer koblet sammen med peptidbindinger som er foldet i en bestemt tredimensionel struktur. Den tredimensionelle struktur er med til at skabe det aktive site, hvor et eller flere meget specifikke substrater passer ind, og kan bindes grundet de intermolekylære bindinger der kan ske mellem de substratet og aminosyrerne i det aktive site. Det er i det aktive site enzymet kan udføre sin funktion. Den tredimensionelle struktur kan også skabe hvad der er kendt som et allosteriske site, som kan ændre strukturen af det aktive site. Når et enzym benyttes som et drug target er vi derfor oftest interesserede i at finde et lægemiddel der kan fungere som substrat i det aktive site eller som kan bindes til det alleosteriske site.
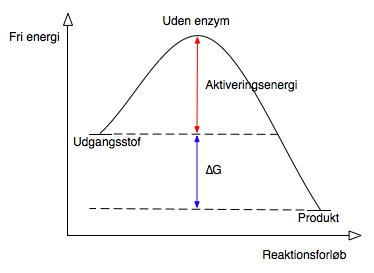
Figur 3. Aktiveringsenergi for en reaktion uden brug af enzym og med brug af enzym. Ved brug af enzym ses en lavere aktiveringsenergi og reaktionen foregår derfor lettere.
Enzymer kan fungere på lidt forskellige måder:
-
Reaktion mellem to molekyler i en opløsning: Enzymet opsamler de to rigtige molekyler og placere dem korrekt i forhold til hinanden, så de har nemmere reagere.
-
Enzymet gør de kovalente bindinger i substratet svagere, da enzymerne trækker i bindingerne. Dette gør en deling af substratet i to lettere.
-
Enzymer kan tilføre midlertidige funktionelle grupper til substratet. Dette sker vha. R-grupperne i enzymet, der kan ”overføre” deres funktionelle gruppe eller dele af dem til substratet. Herefter sker der en række reaktioner, således at enzymets funktionelle grupper bliver gendannet.
Induced fit
Når et substrat nærmer sig et tomt aktivt site på et enzym, interagerer det med enzymet og binder sig. Denne binding fremkalder en konformationsændring i enzymet, som er det, der beskrives som induced fit, se figur 4. Enzymet ændrer form, hvilket gør, at det bedre kan “lukke sig” omkring substratet. Denne ændring skaber de nødvendige bindinger for at katalysere reaktionen.
En vigtig del af denne proces er, at enzymets konformationsændring presser vand ud af det aktive site. Vand kan nemlig interferere med de bindinger, der skal dannes mellem enzymet og substratet (eller target-molekylet). Når vand er til stede, kan det danne hydrogenbindinger med target-molekylet og forhindre dannelsen af nødvendige bindinger til lægemidlet eller substratet.
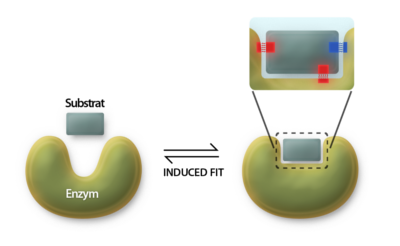
Figur 4. Induced fit: Enzymet tilpasser sig substratet ved en konformationsændring.
Enzymkinetik
Enzymkinetik undersøger, hvordan enzymer reagerer på substrater og påvirkes af faktorer som substrat- og enzymkoncentration, samt hvordan inhibitorer kan hæmme enzymaktivitet. Når man snakker om lægemidler findes der overordnet set to typer:
- Agonister: Binder sig til en receptor eller et enzym og aktiverer det, hvilket fremkalder en biologisk respons, der efterligner den naturlige ligand.
- Antagonister: Binder sig til en receptor eller et enzym, men blokerer effekten af agonister eller naturlige molekyler ved at forhindre deres binding.
Inhibitorer fungerer som enzymernes antagonister. De binder sig til enzymets aktive site og hæmmer dets aktivitet, hvilket sænker reaktionshastigheden. Inhibitorer kan være irreversible (binder kovalent og hæmmer enzymet permanent, som nervegasser eller antabus) eller reversible (binder midlertidigt med ikke-kovalente bindinger), her henvises til illustration på figur 5.
Reversible inhibitorer: Binder midlertidigt til enzymet
- Kompetitiv inhibition: Inhibitoren konkurrerer med substratet om at binde til enzymets aktive site. Øget substratkoncentration kan overkomme hæmningen.
- Ikke-kompetitiv inhibition: Inhibitoren binder til det allosteriske site, hvilket ændrer enzymets tredimentionelle struktur og hæmmer dets aktivitet. Øget substratkoncentration kan ikke overkomme hæmningen.
Irreversible inhibitorer: Binder sig kovalent og permanent til enzymet og inaktiverer det, hvilket ikke kan overvindes ved at øge substratkoncentrationen.
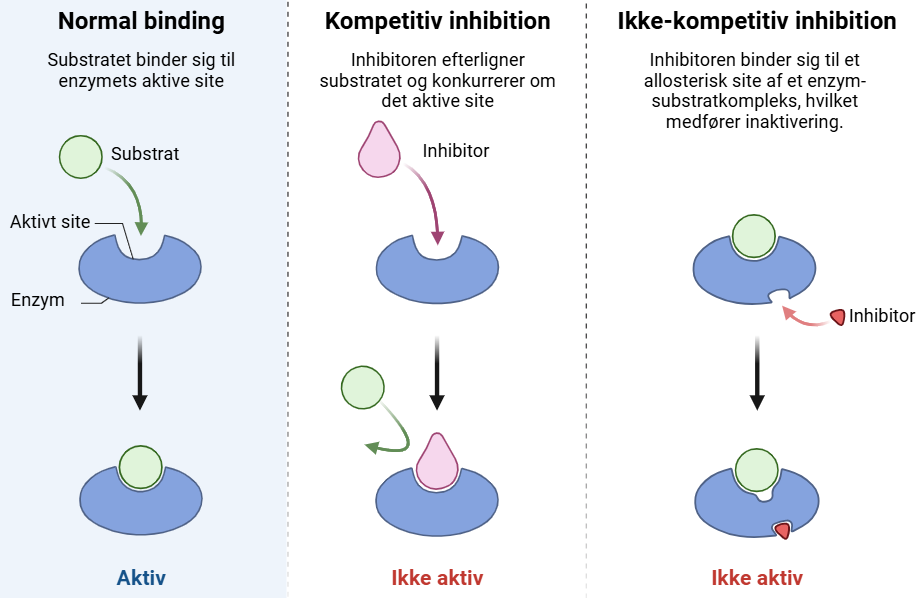
Figur 5. Reversible inhibitorer
Receptorer
Receptorer ligner enzymer i deres opbygning, men er som regel placeret på cellemembranen. Ligesom enzymer indeholder receptorer også en kløft, hvor et molekyle kan binde sig. Kløften kaldes bindingssite, mens det i enzymer kaldes det aktive site. Grunden til, at det hos receptorer ikke kaldes et aktivt site, er, at der oftest ikke sker nogen omdannelse af et udgangsstof i dette område. Når en ligand (som svarer til et substrat for et enzym) binder sig til bindingssitet, sker der en konformationsændring, altså en induced fit. Dette sker hos alle receptorer, men hvad konformationsændringen medfører, kan variere.
G-protein koblede receptorer
Som det kan ses af figur 6, kan konformationsændringen, der opstår ved bindingen af en ligand udefra, medføre, at den del af receptoren, der er inde i cellen, også ændrer sin struktur. Dette resulterer i dannelsen af et nyt bindingssite, der minder om et aktivt site, da det kan fungere som et enzym. En ny ligand (G-protein, bundet til GDP) fra cellens indre kan nu binde sig til det aktive site, hvilket medfører en splitning af G-proteinet inde i cellen. En del af G-proteinet kan derefter sende et signal videre til et membranbundet enzym i cellen, som aktiveres. Hvilke funktioner dette enzym udfører, afhænger af, hvilken type enzym G-proteinet binder sig til. Disse receptorer kaldes G-protein-koblede receptorer.
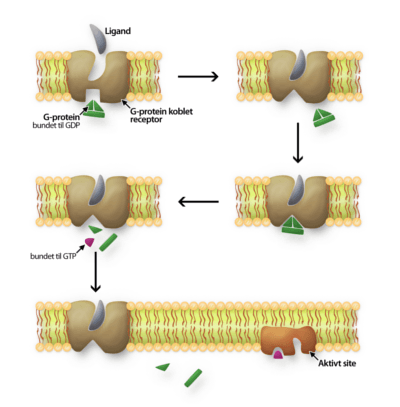
Figur 6. Illustration af mekanismen for en G-protein-koblet receptor. Når en ligand binder sig på ydersiden, ændrer receptoren form og danner et aktivt site på indersiden, hvor et G-protein (bundet til GDP) kan binde sig. G-proteinet splittes, og den del, der binder GTP, aktiverer et membranbundet enzym i cellen.
Ionkanaler
En anden type receptor er ionkanalerne. Disse består ofte af fem protein-subunits, der strækker sig gennem cellemembranen og danner en kanal, som tillader ioner at bevæge sig ind og ud af cellen. De fem subunits er ikke helt ens, da én af dem indeholder et bindingssite. Når en ligand binder sig til dette site, aktiveres ionkanalen, og kanalen åbner sig. Konformationsændringen i ionkanalen sker ved, at subunits trækker sig væk fra midten og danner en kanal (figur 7).
Et lægemiddel, der påvirker en ionkanal, kan virke på to måder: som en blokker eller som en åbner. En blokker holder kanalen lukket og fungerer som en antagonist, mens en åbner holder kanalen åben og fungerer som en agonist.
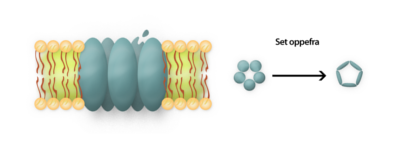
Figur 7. Figuren illustrerer hvordan en iokanal er placeret i en cellemembran og hvordan ionkanalen åbner sig når en ligand bindes til receptoren
Transportproteiner
Transportproteiner er kroppens ”smuglere”, idet de smugler molekyler over cellemembraner, da molekylet i sig selv er for polært til at kunne krydse. Et transportprotein er derfor hydrofobt/upolært på ydersiden, så det kan sidde inde membranen, men er hydrofilt/polært på indersiden, så polære molekyler kan transporteres ind i proteinet. Transportproteinet lukker sig rundt omkring molekylet, der skal transporteres. Herefter bliver det transporteret igennem cellemembranen og sluppet fri på den anden side, se figur 8.
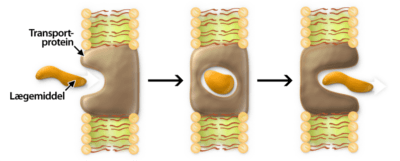
Figur 8. Illustrerer hvordan et lægemiddel kan blive transporteret over en cellemembran via et transportprotein.
Et lægemiddel, der virker på et transportprotein, kan virke på forskellige måder. Lægemidlet kan virke ved selv at blive transporteret over cellemembranen ved at efterligne de molekyler, der normalt transporteres over membranen. Lægemidlet kan også virke ved at blokere transportproteinet og hæmmer derved optagelsen af det stof, som proteinet transporterer. Eksempelvis virker kokain i det centrale nervesystem ved at hæmme genoptagelsen af serotonin og dopamin gennem et transportprotein. Denne hæmning vil medføre, at der vil være mere serotonin og dopamin i synapsekløften mellem de to nerveender, og der vil derfor være et forlænget og øget signal gennem nerverne.
Tolerance og afhængighed
Hvis en celle udsættes for en antagonist i lang tid, vil cellen ikke modtage noget signal fra receptoren. For at kompensere for dette, vil cellen opregulere dannelsen af nye receptorer (figur 9b). Cellen kan nu igen registrere signaler fra den naturlige ligand (figur 9d). For at få den ønskede medicinske virkning vha. antagonisten, er man derfor nødt til at give en højere dosis af lægemidlet (figur 9c). Denne cyklus, hvor cellen danner flere receptorer, og der gives en højere dosis, kan blive ved med at gentage sig. Den tilstand cellen kommer i, og dermed også den tilstand kroppen kommer i, kaldes for tolerance, idet kroppen har brug for mere af lægemidlet for at opnå den ”normale” effekt.
Når indtagelsen af lægemidlet stopper, bliver alle receptorerne frigivet. Dette medfører, at alle de nye receptorer samt de oprindelige vil blive aktiveret af den naturlige ligand (figur 9e). Dette er meget ubehageligt, og man vil føle en trang til at tage stoffet igen, fordi det vil føles som et normalt respons. Dette kaldes for afhængighed, fordi man er nødt til at indtage lægemidlet for at have det godt. Over længere tid vil antallet af receptorer igen falde til et normalt niveau (figur 9f), men indtil da er patienten på afvænning.
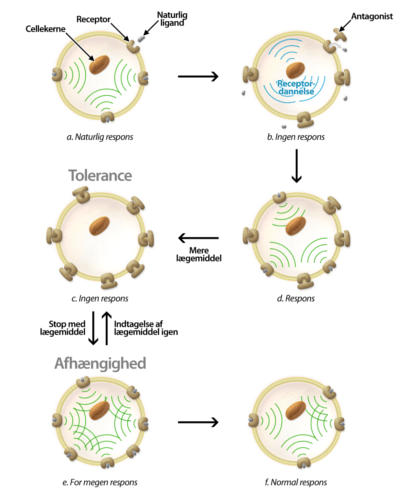
Figur 9. Illustrationen viser hvordan tolerance og afhængighed af et lægemiddel kan forekomme.

