Forløb: Svampe laver din ost
Introduktion: Gennem dette projekt vil du lære om hvordan skimmelsvampe ikke blot er noget der findes i fugtige huse, men faktisk bliver brugt til produktion af en lang række oste. Du vil lære om hvordan bioteknologien benyttes i industrien, og hvordan bioteknologi også er kemi.
Arla Foods amba og Institut for Systembiologi, byder dig velkommen til projektet ”Svampe laver din ost”. Projektet er udarbejdet af Julie Nilsson i samarbejde med de to partnere. Gennem dette projekt vil du lære om hvordan skimmelsvampe ikke blot er noget der findes i fugtige huse, men faktisk bliver brugt til produktion af en lang række oste. Du vil lære om hvordan bioteknologien benyttes i industrien, og hvordan bioteknologi også er kemi. Når du er færdig med projektet, vil du vide hvorfor en ost lugter af ost, og hvorfor blåskimmelost er blå – det er alt sammen svampenes skyld.
Projektet indeholder en række artikler der kan benyttes enkeltvis eller som et samlet undervisningsforløb. Materialet er specielt velegnet til tværfagligt arbejde mellm kemi og biologi, og i særdeleshed også til undervisningen i bioteknologi.
Teorien er suppleret af en eksperimentel øvelse med dyrkning af svampe, der primært henvender sig til biologi og bioteknologi.
Historien om ost
Arla Foods amba og Institut for Systembiologi, byder dig velkommen til projektet ”Svampe laver din ost”. Gennem dette projekt vil du lære om hvordan skimmelsvampe ikke blot er noget der findes i fugtige huse, men også kan bruges positivt som ”starterkulturer” til produktion af en lang række oste. Du vil lære om hvordan bioteknologien benyttes i industrien, og hvordan bioteknologi også er kemi. Når du er færdig med projektet, vil du vide hvorfor en ost lugter af ost, og hvorfor blåskimmelost er blå – det er alt sammen svampenes skyld.
Produktionen af ost menes at kunne dateres flere tusinde år tilbage i tiden, til oldtidsfolket sumererne, der boede i Mesopotamien – det vi nu kender som Irak. Sumererne levede der i år 4.000 – 3.000 f.kr., og således menes osteproduktion at være mere end 5000 år gammel. Både vikingerne omkring år 1000 og senere tiders bønder fremstillede ost, og viden herom kom dels fra egne erfaringer samt fra munke der rejste til Danmark og bragte osteproduktion med sig. I midten af 1800 tallet begyndte man at eksperimentere med en forbedring af mælkeproduktionen, og dette resulterede naturligvis i bedre ostefremstilling.
Med tilsætning af skimmelsvampe til ost, skabtes en ny art ost, nemlig skimmelosten. En af de mest kendte skimmeloste er osten Roquefort. Den produceres af fåremælk i området Roquefort-sur-Soulzon, og tilsættes svampen Penicillium roqueforti (P. roqueforti), der giver blåskimmelosten Roquefort sin karakteristiske smag, duft og udseende. Dernæst lagres osten i de lokale Combalou grotter, hvor jorden allerede indeholder skimmelsvampen P. roqueforti. Dette betyder at svampen har optimale vækstforhold i grotten, da temperaturen og luftfugtigheden er helt perfekt. Udelukkende oste der kommer fra Roquefort-sur-Soulzon området, må kaldes for Roquefort, selv om P. roqueforti anvendes til fremstilling af mange andre blåskimmeloste.
I Danmark begyndte produktionen af blåskimmelost med Hanne Nielsen fra Havartigården, der i 1874 benyttede komælk til produktionen af en Roquefort-lignende ost. Blåskimmelosten HØNG Danablu er udviklet af Marius Boel, der først i 1914 producerede en dansk Roquefort-lignende ost, og dernæst i slutningen af 1920’erne som den første benyttede homogeniseret kaffefløde i produktionen. De skimmelsvampe Marius Boel tilsatte sin ost, voksede han selv frem på gammel rugbrød – hvis mugpletter nemlig også er skimmelsvampe. En ikke helt sikker metode, da Marius ikke kunne være helt sikker på kun at have de godartede skimmelsvampe, men kunne risikere at tilsætte giftige svampe til osten, som kunne vokse under samme betingelser som den gode svamp. I dag sker dyrkningen af skimmelsvampe under kontrollerede forhold i laboratorier, så man er sikret at der kun tilsættes netop den type kultur der ønskes. Hvidskimmeloste som camembert kan dateres tilbage til 1700-tallet, og camembert osten udspringer af den velkendte brieost.
Da man i sin tid begyndte at fremstille skimmeloste, var de kemiske processer bag duft, smag og farveudviklingen ukendte. I dag har mange års forskning betydet, at man nu har viden omkring hvilke kemiske stoffer der giver blåskimmeloste deres karakteristiske smag, og hvad det egentlig er en skimmelsvamp gør ved osten. Gennem introduktion til principperne bag osteproduktion, svampes opbygning og hvordan man kan identificere enkelte kemiske komponenter, der er til stede i en ost, vil du nu få indsigt i hvordan bioteknologien og kemien bruges i vor tids industri.
God fornøjelse.
Teori:
Der er 5 undersider med forskellige teoriafsnit tilknyttet dette projekt. Tryk på knapperne nedenunder for at tilgå dem!
Øvelser:
Øvelse til Svampe laver din ost
Der er en øvelse tilknyttet dette projekt. Det er en eksperimentel øvelse, kaldet Dyrkning af svampe fra ost, hvor eleverne arbejder med at isolere svampe fra skimmeloste indkøbt af underviseren. Disse vokses på YES medie og identificeres vha. en vejledning fundet i undervisningsmaterialet.
Dyrkning af svampe fra ost
Som I kan læse i undervisningsmaterialet ”Svampe laver din ost”, er det yderst vigtigt for osteproducenten Arla Foods, at der ikke er kontaminanter på de oste, der sælges i butikkerne. I skal derfor undersøge, hvilke svampe I kan finde på en ganske almindelig blåskimmelost. Det skal gøres ved at vokse dem i petriskåle og derefter undersøge deres farve, størrelse og sporer.
Der er forskel på, hvor godt svampe vokser på forskellige medier. Derfor skal I prøve at dyrke svampene på to forskellige medier og finde ud af, om svampene gror bedre på det ene end på det andet, og hvorfor.
Forberedelse
Underviseren bedes indkøbe blåskimmeloste, gerne én pr. fire hold. Det er ligeledes nødvendigt at I har et 30 grader inkubatorskab til rådighed, da svampene skal dyrkes ved denne temperatur. Når der laves medie til dyrkningen af svampe, gøres dette jf. opskriften i nedenstående øvelsesvejledning eller se opskriften her på siden.
Klik herunder for at downloade forsøgsvejledningen.
Hvis du har spørgsmål af enhver art til øvelsen, er du meget velkommen til at kontakte Biotech Academy ved at sende en mail på biotech@bio.dtu.dk. Så vil vi forsøge at hjælpe bedst muligt, hurtigst muligt.
Rigtig god fornøjelse!
Her er en oversigt over de to medier vi benytter i forsøget, YES og CYA, og deres komponenter.
Yeast extract – sucrose agar YES
Yeast extract…………… 20.0 g [DIFCO, 0127-01-7]
Sucrose………………… 150 g [BDH, 10274]
MgSO4·7H2O……………. 0.50 g [MERCK, 5886]
Agar……………………… 20.0 g [Bie & Berntsen, BBB 10030, SO-BI-Gel, Agar-Agar]
Spor metaller……………. 1.0 ml
Destilleret vand………. 885 ml
Reguler pH til 6.5 ± 0.1
Czapek yeast extract agar CYA
Yeast extract……………………………. 5.0 g [DIFCO, 0127-01-7]
Czapek Dox Broth (se nedenfor)….. 35.0 g [DIFCO, 0338-01-2]
Agar……………………………………… 15.0 g [Bie & Berntsen, BBB 10030, SO-BI-Gel, Agar-Agar]
Spor metaller……………………………. 1.0 ml
Destilleret vand……………………… 1000 ml
Czapek dox broth (til 1L)
Sucrose…………….. 30.0 g [BDH, 10274]
NaNO3……………….. 3.0 g [MERCK, 6537]
K2HPO4……………… 1.0 g [MERCK, 5099]
KCl…………………… 0.50 g [MERCK, 4936]
MgSO4·7H2O……….. 0.50 g [MERCK, 5886]
FeSO4·7H2O ……….. 0.010 g [MERCK, 3965]
NB! Spormetaller:
Vi kommer altid 1 ml spormetalopløsning i vores medier, så svampene udvikler sig normalt. Dette gør vi fordi man ofte bruger dobbeltdestilleret vand. Derfor tilsættes lidt kobbersulfat og zinksulfat. Det var ikke nødvendigt i gamle dage, da man brugte vand med kobber- og zink-ioner i pga. brugen af kobberrør og forzinkede rør i vandledningssystemet. Svampe har brug for bl.a. kobber ioner for at katalysere polymeriseringen af 1,8-dihydroxynaphthol til melanin, der er det grønne pigment, der beskytter sporerne mod UV lys.
Spormetallerne er som følger:
I 100 ml vand opløses 0.5 g CuSO4 5H2O og 1 g ZnSO4, 7H2O. Af denne opløsning bruge 1 ml til hver liter agar medium.
Oversigt over Penicillum stammer
Identificer svampen vha. dens udseende
Identificer svampen vha. dens sekundære metabolitter, fundet ved TLC
Oversigt over Penicillium stammer
Her finder I en oversigt over en række Penicillium stammer. Stammerne er nummererede, og det givne nummer benyttes videre på siden, hvor I kan finde information om deres udseende på forskellige medier, de metabolitter de producerer m.m.. Oversigten viser nummer, svampens navn og hvem der har opdaget den og hvornår.
1. P. aethiopicum Frisvad 1989
2. P. atramentosum Thom 1910
3a. P. aurantiogriseum Dierckx 1901
3b. P. polonicum Zaleski 1927
3c. P. melanoconidium (Frisvad) Frisvad & Samson 1999
3d. P. neoechinulatum (Frisvad, Filtenborg & Wicklow) Frisvad & Samson 1999
3e. P. viridicatum Westling 1927
3f. P. freii Frisvad & Samson 1999
3g. P. aurantiovirens Biourge 1923
3h. P. tricolor Frisvad, Seifert, Samson & Mills 1994
3i. P. cyclopium Westling 1927
4. P. brevicompactum Dierckx 1901
5a. P. camemberti Thom 1906
5b. P. commune Thom 1906
5c. P. palitans Westling 1911
6a. P. chrysogenum Thom 1910
6b. P. dipodomyis (Frisvad, Filtenborg & Wicklow) Frisvad 1997
6c. P. nalgiovense Laxa 1932
7. P. clavigerum Demelius 1922
8. P. confertum (Frisvad, Filtenborg & Wicklow) Frisvad 1989
9. P. coprophilum (Berk. & Curt.) Seifert & Samson 1985
10. P. coprobium Frisvad 1989
11. P. crustosum Thom 1930
12. P. digitatum (Pers.:Fr.) Sacc. 1832 (Predominantly one-stage branched)
13a. P. echinulatum Fassatiová 1977
13b. P. discolor Frisvad & Samson 1997
14a. P. expansum Link 1809
14b. P. formamosanum Hsieh, Su & Tzean 1987
16a. P. glandicola (Oud.) Seifert & Samson 1985
16b. P. concentricum Samson, Stolk & Hadlok 1976
17a. P. griseofulvum Dierckx 1901
17b. P. dipodomyicola (Frisvad, Filtenborg & Wicklow) Frisvad 1999
18a. P. hirsutum Dierckx 1901
18b. P. albocoremium (Frisvad) Frisvad 1999
18c. P. allii (Vincent & Pitt) Frisvad 1989
18d. P. hordei Stolk 1969
18e. P. venetum (Frisvad) Frisvad 1999
19a. P. italicum Wehmer 1894
19b. P. ulaiense Hsieh, Su & Tzean 1987
20. P. solitum Westling 1911
21. P. mononematosum (Frisvad, Filtenborg & Wicklow) Frisvad 1989
22. P. olsonii Bain. & Sart. 1912
23a. P. roqueforti Thom 1906
23b. P. carneum (Frisvad) Frisvad 1996
23c. P. paneum Frisvad 1996
24a. P. nordicum Dragoni & Cantoni ex Ramírez 1986
24b. P. verrucosum Dierckx 1901
25. P. vulpinum (Cooke & Massee) Seifert & Samson 1985
26. P. sclerotigenum Yamamoto 1955 (Predominantly one-stage branched)
27. P. oxalicum Currie & Thom 1915 (Predominantly one-stage branched)
Først ser vi på hvordan svampene ser ud. Når I har målt deres diameter, kan I gå ind i oversigten herunder, og finde ud af hvilke mulige svampe det er I har vokset frem. Herefter ser I på hvilke farver svampene har, og benytter oversigten “Makromorfologiske kendetegn og farver” ligeledes herunder, til igen at pejle jer ind på hvilken svamp I har. Endelig skal I se på mikromorfologiske kendetegn og metabolitter produceret.
Fysiologiske kendetegn
Her er størrelsen af svampene præsenteret efter 7 dages vækst ved 25 grader. En svamp kan være repræsenteret i flere forskellige størrelses-intervaller.
Koloni diametre (efter 7 dage ved 25°C):
På CYA:
< 15 mm: 7, 3i, 24a, 24b
15-19 mm: 3a, 3e, 3f, 3g, 3i, 4, 5a, 5b, 6c, 7, 9, 10, 12, 14b, 16a, 16b, 17a, 20, 21, 24a, 24b
20-24 mm: 2, 3a, 3c, 3e, 3f, 3g, 3i, 4, 5a, 5b, 5c, 6a, 6c, 7, 8, 9, 10, 12, 13b, 14b, 16a, 16b, 17a, 18e, 19a, 20, 21, 24a, 24b, 25
25-29 mm: 1, 2, 3a, 3b, 3c, 3e, 3f, 3g, 3i, 4, 5a, 5b, 6a, 6b, 6c, 8, 9, 10, 12, 13a, 13b, 14b, 16a, 16b, 17a, 18a, 18b, 18c, 18d, 18e, 19a, 20, 21, 22, 25
30-34 mm: 1, 2, 3a, 3b, 3e, 3f, 4, 5a, 5b, 5c, 6a, 6b, 6c, 9, 11, 12, 13a, 13b, 14a, 14b, 16a, 18a, 18b, 18c, 18d, 18e, 19a, 20, 21, 22, 23a, 23b, 25
35-39 mm: 1, 2, 3b, 3e, 5b, 5c, 6a, 11, 13a, 13b, 14a, 14b, 16a, 18a, 18b, 18c, 18d, 19a, 22, 23a, 23b, 23c, 25
40-45 mm: 2, 3b, 6a, 11, 14a, 14b, 18b, 18d, 19a, 23a, 23b, 23c, 25, 26
46-50 mm: 6a, 11, 14a, 23a, 23b, 23c, 26
> 51 mm: 23a, 23b, 23c, 26
På YES:
< 20mm: 7, 24a, 24b
20-24 mm: 3c, 3e, 3f, 4, 6c, 7, 16a, 24a, 24b
25-29 mm: 3a, 3c, 3e, 3f, 3g, 3i, 4, 5a, 5b, 6c, 8, 9, 10, 12, 16a, 16b, 17a, 21, 24a, 24b, 25
30-34 mm: 1, 2, 3a, 3b, 3c, 3e, 3f, 3g, 3i, 4, 5a, 5b, 6c, 7, 8, 9, 10, 12, 13a, 13b, 14b, 16a, 16b, 17a, 20, 21, 24a, 24b, 25
35-39 mm: 1, 2, 3a, 3b, 3c, 3e, 3f, 3g, 3i, 4, 5a, 5b, 5c, 6c, 8, 9, 10, 11, 12, 13a, 13b, 14b, 16a, 17a, 18b, 18c, 18d, 18e, 19a, 20, 21, 25
40-44 mm: 1, 2, 3a, 3b, 3e, 3g, 3i, 5a, 5b, 5c, 6a, 6c, 9, 11, 12, 13a, 13b, 14a, 14b, 16a, 18a, 18b, 18c, 18d, 18e, 19a, 20, 21, 22, 25
45-50 mm: 1, 2, 3b, 5b, 5c, 6a, 6c, 9, 11, 12, 13a, 13b, 14a, 14b, 16a, 18a, 18b, 18c, 18d, 18e, 19a, 20, 22, 23b, 25
51-55 mm: 1, 2, 6a, 11, 12, 13a, 13b, 14a, 14b, 18b, 18c, 19a, 22, 23a, 23b, 23c, 26
56-60 mm: 1, 2, 6a, 11, 12, 14a, 18b, 19a, 22, 23a, 23b, 23c, 26
61-65 mm: 2, 6a, 12, 14a, 18b, 19a, 23c, 26
> 65 mm: 18b, 19a, 23a, 23b, 23c, 26
Makromorfologiske kendetegn og farver
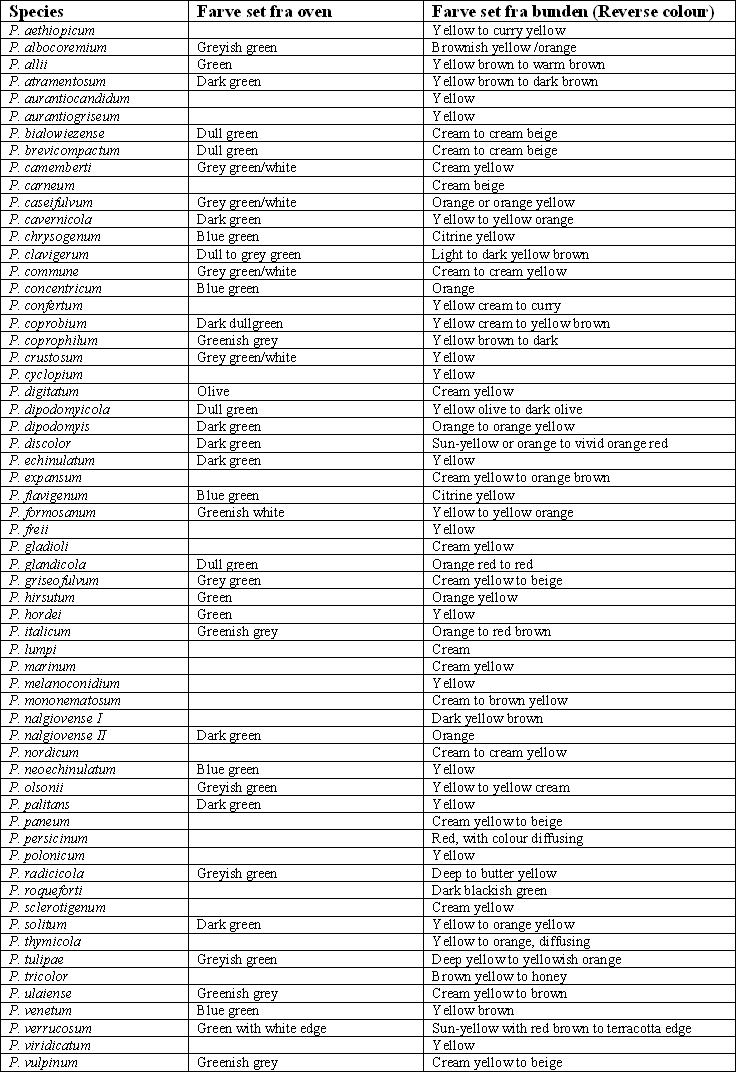
Mikromorfologiske kendetegn
Hvis I vil se på svampene under mikroskop, følger her en liste over sporernes udseende på de enkelte svampe.
Conidia:
Cylindriske og rundede ender: 12, 19a, 19b
Elliptiske: 1, (3a), (3b), 4, (5b), (5c), (6a), 7, 8, 9, 10, 12, 14a, 14b, 16a, 16b, 17a, 17b, 19a, 19b, (20),21, 22, 25, 26, 27
Echinulate: 3d, 13a, 13b
Let ru: 4, 18d, (20), 22,
> 3.5 µm long: 12, 19a, 19b, 26, 27
Phialides:
< 6.5 µm long: 17a, 17b
Kort med bred tyk hals: 6a, 6b, 6c, 21
Rami:
Divergent: 2, 6a, 6b, 6c, (8), (12), 17a, (18d), 21,
Højt antal: 22
Få eller ikke til stede: 12, 26, 27
Supplerende koloni-kendetegn for Penicillium
P. aethiopicum: Stærkt pliceret revers på CYA og YES. Gult revers på CYA. Stængler typisk ru på MEA, men glatte på CYA.
P. albocoremium: Hvide synnemata på MEA. Vatagtig koloni på CYA.
P. allii: Korte meget ru stængler. Flade kolonier.
P. atramentosum: Rødbrunt revers på CYA.
P. aurantiogriseum: Tydeligt blå (grønne) konidier på MEA. Ofte grålige og ellipsoide konidier på CYA.
P. aurantiovirens: Flokkøs på MEA, vattet mycelie-rand, mange exudat-dråber, blå (grønne) konidier på MEA.
P. brevicompactum: Penicilli kompakte, opsvulmede for enden af stængel og metulae. Phialiderne spredt ud som en vifte, ligner overfladisk ligner en Aspergillus.
P. camemberti: Hvide vattede kolonier på alle substrater.
P. carneum: Flødefarvet til lysebrunt revers på CYA. Kan gro på 0.5 % edddikesyre. Gror godt på nitrit agar. Lugter kraftigt af ‘mug’.
P. chrysogenum: Ofte gule exudatdråber og revers på CYA. Tynde kolonier på MEA. Næsten altid store kolonier på alle substrater.
P. clavigerum: Nåleformede indeterminate synnemata. Brungult revers CYA.
P. commune: Oftest svag sporulation YES. Flødefarvet revers, der bliver brunt til sortbrunt med tiden på YES i mange, dog ikke alle isolater.
P. concentricum: Blågrønne konidier på MEA, orange revers på MEA. Af og til tændstikformede synnemata på MEA.
P. coprobium: Mørkegrønne konidier på CYA. Af og til små hvide sclerotier på MEA. Konidier i koncentriske ringe på CYA.
P. coprophilum: Mørkebrunt revers CYA. Meget ujævn kolonimargen på især MEA.
P. crustosum: Konidier dannes i så stort tal at der efter 7-14 dage dannes skorper.
P. cyclopium: (grå)grøn på CYA, men blå grå grøn på MEA, stærkt gult obvers og flad koloni på YES.
P. digitatum: Konidier (olivenfarvede) er usædvanligt store og af varieret form og størrelse. Penicilli er ofte fragmentariske med kun to delepunkter.
P. discolor: Meget mørkegrønne konidier på alle substrater, revers på YES bliver orange til kraftig rødt efter 7-14 dage.
P. echinulatum: Meget mørkegrønne konidier på alle substrater.
P. expansum: Ret “høje” kolonier, lidt vatagtige. Ofte klare eller brune exudatdråber på CYA. Brunligt revers på CYA. Af og til synnemata (tændstikformede) på MEA.
P. freii: Store klare exudat-dråber på CYA, særlig stærk sporeproduktion på CYA.
P. glandicola: Rødorange revers på MEA, fjeragtige synnemata på MEA.
P. griseofulvum: Meget små phialider (< 6.5 mm) med korte halse.
P. hirsutum: Gulbrunt revers og exudatdråber på CYA. Ofte gule tændstikformede synnemata på MEA.
P. hordei: Vatagtig på CYA med gult mycelium. Gule synnemata (fjeragtige) på MEA.
P. italicum: Brunrødt revers på CYA. (P. ulaiense forekommer på citrus frugter,den vokser langsomt på CYA, har flødefarvet revers og tydelige hvide synnemata)
P. melanoconidium: Mørkegrønne konidier på CYA, men blågr¢nne konidier på MEA. Gult revers på CYA.
P. nalgiovense: Orange revers på MEA. Hvide eller lyst grågrønne konidier. Konidier kan dog også være mørkt grønne. Indtil videre kun fundet på salami.
P. nordicum: Flødefarvet revers på YES. Langsomtvoksende på CYA og MEA. Rent grønne konidier.
P. olsonii: Meget lange stilke med multiramulate penicilli. Ligner overfladisk en Aspergillus i stereomikroskop.
P. palitans: Stærk sporulation på YES, grønne konidier. Gul til gulorange revers. Mørkegrønne konidier på CYA.
P. paneum: Hurtigtvoksende på alle substrater. Flødefarvet til lysebrunt revers på CYA. Kan gro på 0.5 % edddikesyre. Gror godt på nitrit agar.
P. polonicum: Stor flad koloni på CYA med blågrønne konidier
P. roqueforti: Kan gro på 0.5 % edddikesyre. Gror godt på nitrit agar. Mørkegrønt revers på CYA. Spindelvævsagtig tynd kolonimargin på CYA og MEA.
P. sclerotigenum: Sclerotier på MEA. Hidtil kun fundet på yams.
P. solitum: Mørkegrønne konidier på CYA. Flødefarvet revers på CYA ofte med brun midte.
P. venetum: Stærktfarvet brun + bananfarvet revers på CYA, blågrønne konidier. Ret lav væksthastighed.
P. verrucosum: Gullig til flødefarvet revers på CYA, kraftig rødbrunt til violetbrunt revers på YES. Langsomtvoksende på CYA og MEA. Rent grønne konidier.
P. viridicatum: Rent grønne konidier på alle substrater.
P. vulpinum: Store tændstikformede synnemata på CYA og MEA.
Produktionen af sekundære metabolitter detekteret ved TLC
Herunder ser I en liste over sekundære metabolitter, og de svampe der producerer dem.
3-methoxyviridicatin: 3b, 3d, 3f, 3g, 3i, 18b, 18c, 18e
Aurantiamine: 3a, 3f, 3d
Brevianamide A: 3e, (4)
Chaetoglobosin C: 14a, 13b
Chrysogine: 6a, 6b, 6c, 18b
Citrinin: 14a, 18b, 24b
Compactin A & B: 18a, (20)
Cyclopaldic acids: (5a), 5b, 21, (23b)
Cyclopenin & Cyclopenol: 3b, 3d, 3f, 3g, 3i, (5c), 11, 13a,13b,18b, 18c, 18e, 20, 25
Cyclopiazonic acid: 5a, 5b, 5c, (7), 17a, 17b
Griseofulvin: 1, 9, 17a, 17b, 26
Isofumigaclavine A: 5c, 7, 23a, 23b
Meleagrin: (2), 6a, 8, 9, 10, 16a, 16b, 18b, 18c, (25)
Met O: 4, 22
Mycophenolic acid: 4, (23a), 23b
Ochratoxin A: 24a, 24b
Oxaline: 2, 3c, 9, 16a, 25, 27
Penicillic acid: 3a, 3b, 3c, 3d, (3e), (3f), 3g, 3i, 18b,(23b)
Penitrem A: 3c, 7, 11, 16a, (16b), 18b, 23b
Raistrick phenols: 4
Roquefortine C: (2), 6a, (7), 8, 9, (10), 11, 14a, 16a, 16b,17a,18a, 18b, 18c, 18e, 23a, 23b, 23c, 25, 26, (27)
Rugulovasine A & B: 2, (5a), 5b
Terrestric acid: 3a, 3h, 11, 18a, 18b, 18d, 18e
Territrems: 13a
Verrucosidin: 3a, 3b, 3c
Viomellein: (3c), 3e, 3f, 3h, 3i, (7)
Viridamine: 3e
Viridicatin: (5c), 11, 13a, 13b, 20, 25
Xanthomegnin: (3c), 3e, 3f, 3h, 3i, (7)
Metabolitnøgle for Penicillium metabolitter
Denne tabel viser Rf værdierne for en række forskellige metabolitter, når der benyttes hhv. TEF og CAP som løbevæske ved TLC’en. Herudover forklares plettens farve på TLC pladen under forskellige behandlinger.
|
Rf værdi: TEF/CAP |
Før spray |
AlCl3 |
Ce(SO)4 |
ANIS |
|
|
3-methoxyviridicatin |
154 / 88 |
blå |
blå |
blå |
blå |
|
Aurantiamin |
31 / 80 |
blå |
blå |
grå |
grå |
|
Brevianamide A |
71 / 86 |
gul-grøn |
gul |
orangeVIS |
grå-gul |
|
Chaetoglobosin C |
111 / 80 |
mørk |
mørk |
mørk |
brun |
|
ChrysoginY |
62 / 28 |
blå254 |
blå |
grå |
grå |
|
CitrininY |
126H / 15H |
gul-grøn |
gul |
gul |
lys gul |
|
Compactin A & BY |
54+94 / 54+104 |
DI |
DI |
DI |
gul-brun |
|
Cyclopaldic acidsY |
77+146 / 54 |
svag blå254 |
turkis |
turkis |
lys turkis |
|
Cyclopenin |
111 / 94 |
DI |
violetVIS |
grå |
grå |
|
Cyclopenol |
82 / 79 |
DI |
grå-blåVIS |
grå |
grå |
|
Cyclopiazonic acid |
130H / 17H |
brun |
blå-brun |
lys |
lys brun |
|
Griseofulvin |
100 / 100 |
blå |
grå |
grå |
lys blå |
|
(Iso)fumigaclavine A |
7 / 33 |
grå |
grå |
grå |
brun |
|
Meleagrin/Oxaline |
4 / 74 |
DI |
brun-gulVIS+365 |
||
|
Met O |
120 / 125 |
gul-grøn254 |
gul |
gul |
gul |
|
Mycophenolic acid |
135 / 85 |
blå254 |
blå |
blå |
blå |
|
Ochratoxin A |
153 / 23 |
blå-grøn |
blå-grøn |
blå-grøn |
blå-grøn |
|
Penicillic acidY |
103 / DI |
DI |
DI |
DI |
rød-blå |
|
Penitrem A |
189 / 120 |
DI |
blå-sortVIS+365 |
||
|
Raistrick phenols |
87/35 |
blå254 |
blå |
blå |
blå |
|
Roquefortine C |
0 / 46 |
DI |
DI |
orangeVIS |
mørkVIS |
|
Rugulovasine A & B |
11 / 22+50 |
grå-blå |
grå-blå |
grå |
grå |
|
Terrestric acidY |
106H / 100 |
DI |
DI |
DI |
gulVIS |
|
Territrems |
85+115+140 / 112+96+85 |
blå |
blå |
blå |
blå |
|
Verrucosidin |
144 / DI |
DI |
DI |
DI |
brun-gul |
|
Viomellein |
106 / 104 |
gul-brunVIS |
gul-brunVIS |
DI |
mørk |
|
Viridamine |
20 / 46 |
lys blå |
blå |
blå |
blå |
|
Viridicatin |
154 / 77H |
svag blå254 |
violet |
grå-blå |
grå-blå |
|
Xanthomegnin |
74 / 80 |
gul-brunVIS |
gul-brunVIS |
DI |
mørk |
Y Metabolitterne dannes bedst på YES; H Metabolitterne ses ikke som veldefinerede pletter, men som haler.; DI Detekteres ikke under de givne betingelser; 365 Farven ses under UV lys 365 nm; 254 Farven ses under UV lys 254 nm; VIS Farven ses ved synligt lys.
Kendte Penicillium metabolitter detekteret via TLC
Denne oversigt beskriver hvilke metabolitter de enkelte Penicillium stammer producerer. Den kan også benyttes til at identificere svampe med.
P. aethiopicum: Griseofulvin
P. albocoremium: Citrinin, (penicillic acid), meleagrin, roquefortine C, terrestric acid, viridicatins, penitrem A
P. allii: meleagrin, Roquefortine C, viridicatin
P. atramentosum: (Meleagrin), oxaline, (roquefortine C), rugulovasine
P. aurantiogriseum: Aurantiamine, penicillic acid, terrestric acid, verrucosidin
P. aurantiovirens: 3-methoxyviridicatins, penicillic acid
P. brevicompactum: Brevianamide, mycophenolic acid, met. O, raistrick phenols
P. camemberti: Cyclopiazonic acid
P. carneum: Isofumigaclavin A, (cyclopaldic acid), mycophenolic acid, (penicillic acid), penitrem A, roquefortine C,
P. chrysogenum: Roquefortine C, chrysogine, meleagrin
P. clavigerum: (Meleagrin), penitrem A, (roquefortine C), (viomellein)
P. commune: Cyclopaldic acid, cyclopiazonic acid, rugulovasine
P. concentricum: Meleagrin, (penitrem A), roquefortine C
P. coprobium: Patulin, (roquefortine C), (meleagrin)
P. coprophilum: Griseofulvin, meleagrin, oxaline, roquefortine C
P. crustosum: Penitrem A, roquefortine C, terrestric acid, viridicatins
P. cyclopium: 3-methoxyviridicatins, penicillic acid, xanthomegnin, viomellein
P. discolor: Chaetoglobosins, viridicatins
P. echinulatum: Territrems, viridicatins
P. expansum: Roquefortine C, chaetoglobosins, citrinin
P. freii: Aurantiamine, xanthomegnin, viomellein, 3-methoxyviridicatins
P. glandicola: Meleagrin, oxaline, penitrem A, roquefortine C
P. griseofulvum: Cyclopiazonic acid, fulvic acids, griseofulvin, roquefortine C
P. hirsutum: Compactins, roquefortine C, terrestric acid
P. hordei: Roquefortine C, terrestric acid, (viridicatins)
P. melanoconidium: Oxaline, penicillic acid, penitrem A, verrucosidin, (viomellein), (xanthomegnin)
P. nalgiovense: (Chrysogine)
P. nordicum: Ochratoxin A, verrucolone
P. olsonii: Met. O
P. palitans: Cyclopiazonic acid, (viridicatins), isofumigaclavine A,
P. paneum: Roquefortine C
P. polonicum: Penicillic acid, verrucosidin, 3-methoxyviridicatins
P. roqueforti: (Mycophenolic acid), isofumigaclavin A, roquefortine C
P. sclerotigenum: Griseofulvin, roquefortine C
P. solitum: Compactins, viridicatins
P. venetum: Roquefortine C, terrestric acid, viridicatins
P. verrucosum: Ochratoxin A, citrinin, verrucolone
P. viridicatum: Brevianamide A, viomellein, viridamine, xanthomegnin
P. vulpinum: Meleagrin, oxaline, roquefortine C, viridicatins
Herunder ser I TLC billeder af en række Penicillium svampe ved forskelligt UV lys og fremkaldt med forskellige reagenter. Se teksten under billedet for at se omtalte betingelser. Billederne er venligst udlånt af mykologi gruppen ved DTU Systembiologi.





















Kildehenvisning:
Dette projekt blev udgivet i november 2010. Det er udarbejdet af Biotech Academy og er blevet opdateret løbende.

Kristian Fog Nielsen er lektor ved DTU Systembiologi og arbejder med mikrobiologi og analytisk kemi. Kristian har assisteret ved udarbejdelsen af projektet Svampe laver din ost.
Kristian Fog Nielsen

Jens Christian Frisvad er professor ved DTU Systembiologi og arbejder med svampe og deres kemiske diversitet. Jens har assisteret ved udarbejdelsen af øvelsen til Svampe laver din ost.
Jens Christian Frisvad

Institut for Systembiologi har Danmarks største biovidenskabelige og bioteknologiske forskning på universitetsniveau.
Instituttet har været partner og sponsor på projektet.




